
Категории:
ДомЗдоровьеЗоологияИнформатикаИскусствоИскусствоКомпьютерыКулинарияМаркетингМатематикаМедицинаМенеджментОбразованиеПедагогикаПитомцыПрограммированиеПроизводствоПромышленностьПсихологияРазноеРелигияСоциологияСпортСтатистикаТранспортФизикаФилософияФинансыХимияХоббиЭкологияЭкономикаЭлектроника
Закон сохранения массы и энергии
Фундаментальным законом естествознания является закон сохранения массы вещества, который был сформулирован в 1748 г. в виде философской концепции великим русским ученым М.В. Ломоносовым (1711–1765) и подтвержден экспериментально им самим в 1756 г., а также независимо от него - французским химиком А.Л. Лавуазье в 1789 г.
Закон сохранения массы вещества гласит: масса веществ, вступающих в химическую реакцию, равна массе всех продуктов реакции.
Опыты по сжиганию веществ, которые проводились до Ломоносова, наводили на мысль, что масса веществ в процессе реакции не сохраняется. При нагревании на воздухе ртуть превращалась в красную окалину, масса которой была больше массы металла. Масса золы, образующейся при сгорании дерева, напротив, всегда меньше массы исходного вещества. Немецкий врач и химик Эрнст Шталь (1660–1734) пытался объяснить эти явления тем, что горючие вещества содержат некоторую субстанцию – флогистон, которая в процессе горения улетучивается или передается от одного вещества к другому. Это означало, что горение вещества есть реакция разложения на флогистон и негорючий остаток. Но тогда получалось, что есть положительный флогистон (содержится в дереве), который приводит к уменьшению массы при горении, и отрицательный (в металлах), который дает увеличение массы.
Ломоносов провел простой опыт, который показал, что горение металла есть реакция присоединения, а увеличение массы металла происходит за счет присоединения части воздуха. Он прокаливал металлы в запаянном стеклянном сосуде и обнаружил, что масса сосуда не изменялась, хотя химическая реакция происходила.
К сожалению, открытие Ломоносова не было замечено зарубежными учеными, а закон сохранения массы вещества утвердился в химии только после опытов Лавуазье, который проводил реакции сжигания металлов и восстановления оксидов металлов углем, и ни разу не обнаружил увеличения или уменьшения массы продуктов реакции по сравнению с исходными веществами.
Закон сохранения массы вещества имел огромное значение для атомно-молекулярной теории. Он подтвердил, что атомы являются неделимыми и при химических реакциях не изменяются. Молекулы при реакции обмениваются атомами, но общее число атомов каждого вида не изменяется и поэтому общая масса веществ в процессе реакции сохраняется. Закон сохранения массы вещества является частным случаем общего закона природы - закона сохранения энергии, который утверждает, что энергия изолированной системы постоянна. Энергия – это мера движения и взаимодействия различных видов материи. При любых процессах в изолированной системе энергия не производится и не уничтожается, она может переходить из одного вида в другой. Например, энергия электромагнитного излучения, действующего на молекулу, может переходить в энергию вращательного движения молекулы или поступательного движения атомов; напротив, энергия химического взаимодействия может переходить в энергию излучения.
Закон сохранения энергии как философский принцип не выводится из более общих постулатов. С физической точки зрения закон сохранения энергии является следствием однородности времени, т.е. того факта, что законы природы со временем не меняются.
Закон сохранения массы вещества не выполняется в ядерных реакциях, что объясняется на основе принципа эквивалентности массы и энергии, сформулированного Эйнштейном и выражаемого самой знаменитой в мире формулой: Е = mc2.
Это соотношение показывает, что масса может переходить в энергию и наоборот, что и происходит в ядерных реакциях. В химических реакциях изменение массы, вызванное выделением или поглощением энергии, очень мало и не поддается экспериментальной регистрации. Поэтому можно утверждать, что в химических реакциях закон сохранения массы выполняется с очень высокой степенью точности.
Периодический закон Менделеева
Утверждение атомно-молекулярной теории на рубеже XVIII–XIX вв. сопровождалось бурным ростом числа известных химических элементов. Только за первое десятилетие XIX в. было открыто 14 новых элементов. Английский химик Г. Дэви (1778–1829) за один год с помощью электролиза получил шесть новых элементов– натрий, калий, магний, кальций, стронций, барий. К 1830 г. число известных элементов достигло 55.
Существование такого количества элементов, весьма разнообразных по свойствам, озадачивало химиков и требовало систематизации элементов. Некоторые ученые, заметив сходства нескольких элементов, объединяли их в отдельные группы, однако причины заметного изменения свойств не были установлены. Периодический закон химических элементов – фундаментальный закон природы – был открыт великим русским химиком Д.И. Менделеевым в 1869 г. в результате систематизации химических элементов в зависимости от их атомных весов: свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величины атомных весов элементов.
Несмотря на огромную значимость открытия Менделеева, оно представляло лишь гениальное эмпирическое обобщение фактов, а их физический смысл долго оставался непонятным. Причина заключалась в том, что в XIX в. отсутствовали какие-либо представления о сложном строении атома. Сам Менделеев по этому поводу писал: "Периодическая изменяемость простых и сложных тел подчиняется некоторому высшему закону, природу которого, а тем более причину еще нет средств охватить. По всей вероятности, она кроется в основных началах внутренней механики атомов и частиц".
Данные о строении атомного ядра и распределении электронов в атомах позволяют по-новому рассмотреть периодический закон, который в современной формулировке гласит: свойства простых веществ, а также формы и свойства соединений элементов находятся в периодической зависимости от заряда ядра атомов (порядкового номера).
Такая формулировка закона не противоречит формулировке, данной Менделеевым. Она только базируется на новых данных, которые придают закону физическую обоснованность, и подтверждают его правильность. Примерами, иллюстрирующим проявление периодического закона химических элементов, может служить периодическая зависимость плотности простых веществ в твердом состоянии от порядкового номера элемента (заряда ядра), или же такие характеристики атома как его размер, энергия ионизации, электроотрицательность, степень окисления, имеющие периодическую зависимость от заряда атомного ядра (рис. 4.3).
Табличной формой представления периодического закона является периодическая система химических элементов, разработанная Менделеевым в 1869–1871 гг.

Рис. 4.3. Зависимость плотности простых веществ в твердом состоянии от порядкового номера.
В периодической системе химических элементов все известные в настоящее время химические элементы расположены в порядке возрастания зарядов их атомных ядер, численно равных порядковому номеру элемента, и образуют 7 горизонтальных периодов, каждый из которых, за исключением первого, начинается щелочным металлом и заканчивается инертным газом, причем, седьмой период является незавершенным. Первые три периода, состоящие из одного ряда, называются малыми, остальные – большими.
 По вертикали химические элементы располагаются в 8 вертикальных столбцах-группах, причем каждая группа делится на две подгруппы – главную, состоящую из элементов второго и третьего периодов и сходных с ними элементов больших периодов, и – побочную, состоящую из металлов больших периодов. Отдельно внизу таблицы помещены элементы с порядковыми номерами 58–71, называемые лантаноидами, и – элементы с порядковыми номерами 90–103, называемые актиноидами. В каждой клетке периодической системы химических элементов, помимо наименования элемента и его порядкового номера, приведено значение относительной атомной массы элемента и показано распределение электронов по энергетическим уровням (рис. 4.4).
По вертикали химические элементы располагаются в 8 вертикальных столбцах-группах, причем каждая группа делится на две подгруппы – главную, состоящую из элементов второго и третьего периодов и сходных с ними элементов больших периодов, и – побочную, состоящую из металлов больших периодов. Отдельно внизу таблицы помещены элементы с порядковыми номерами 58–71, называемые лантаноидами, и – элементы с порядковыми номерами 90–103, называемые актиноидами. В каждой клетке периодической системы химических элементов, помимо наименования элемента и его порядкового номера, приведено значение относительной атомной массы элемента и показано распределение электронов по энергетическим уровням (рис. 4.4).



Рис. 4.4. Фрагмент периодической системы химических элементов.
На основе периодического закона химических элементов и периодической таблицы Менделеев пришел к выводу о существовании новых элементов, свойства которых он подробно описал и дал им условные названия – экабор, экаалюминий и экасилиций. Предсказания Менделеева блестяще подтвердились, – все три элемента были открыты и получили названия тех стран, где были сделаны открытия и найдены минералы, содержащие эти элементы: галлий, скандий, германий. Таким образом, Менделеев провел блестящий теоретический анализ огромного числа экспериментальных данных, синтезировал свои результаты в виде общего закона и сделал на его основе предсказания, которые вскоре были подтверждены экспериментально. Эта работа является классическим примером научного подхода к познанию окружающего мира.
Электронное строение атома
Так как при химических реакциях ядра реагирующих атомов остаются без изменений (за исключением радиоактивных превращений), то химические свойства атомов зависят от строения их электронных оболочек. Теория электронного строения атома построена на основе аппарата квантовой механики. Так, структура энергетических уровней атома может быть получена на основе квантовомеханических расчетов вероятностей нахождения электронов в пространстве вокруг атомного ядра (рис. 4.5).

Рис. 4.5. Схема подразделения энергетических уровней на подуровни
Основы теории электронного строения атома сводятся к следующим положениям: состояние каждого электрона в атоме характеризуется четырьмя квантовыми числами: главным квантовым числом n = 1, 2, 3, ¼; орбитальным (азимутальным) l=0,1,2,¼n–1; магнитным ml = –l,¼–1,0,1,¼l; спиновым
ms = -1/2, 1/2.
Согласно принципу Паули, в одном и том же атоме не может быть двух электронов, обладающих одинаковой совокупностью четырех квантовых чисел n, l, ml, ms ; совокупности электронов с одинаковыми главными квантовыми числами n образуют электронные слои, или энергетические уровни атома, нумеруемые от ядра и обозначаемые как K, L, M, N, O, P, Q, причем в энергетическом слое с данным значением n могут находиться не более, чем 2n2 электронов. Совокупности электронов с одинаковыми квантовыми числами n и l , образуют подуровни, обозначаемые по мере удаления их от ядра как s, p, d, f .
Вероятностное нахождение положения электрона в пространстве вокруг атомного ядра соответствует принципу неопределенностей Гейзенберга. По квантовомеханическим представлениям, электрон в атоме не имеет определенной траектории движения и может находиться в любой части пространства вокруг ядра, а различные его положения рассматриваются как электронное облако с определенной плотностью отрицательного заряда. Пространство вокруг ядра, в котором наиболее вероятно нахождение электрона, называется орбиталью. В нем заключено порядка 90% электронного облака. Каждому подуровню 1s, 2s, 2p и т.д. соответствует определенное количество орбиталей определенной формы. Например, 1s- и 2s-орбитали имеют сферическую форму, а 2p-орбитали (2px, 2py, 2pz-орбитали) ориентированы во взаимно перпендикулярных направлениях и имеют форму гантели (рис. 4.6).
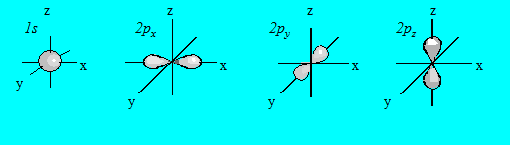
Рис. 4.6. Форма и ориентация электронных орбиталей.
При химических реакциях атомное ядро не претерпевает изменений, изменяются лишь электронные оболочки атомов, строением которых объясняются многие свойства химических элементов. На основе теории электронного строения атома был установлен глубокий физический смысл периодического закона химических элементов Менделеева и создана теория химической связи.
Теоретическое обоснование периодической системы химических элементов включает в себя данные о строении атома, подтверждающие существование связи между периодичностью изменения свойств химических элементов и периодическим повторением сходных типов электронных конфигураций их атомов.
В свете учения о строении атома становится обоснованным разделение Менделеевым всех элементов на семь периодов: номер периода соответствует числу энергетических уровней атомов, заполняемых электронами. В малых периодах с ростом положительных заряда ядер атомов возрастает число электронов на внешнем уровне (от 1 до 2 в первом периоде, и от 1 до 8 во втором и третьем периодах), что объясняет изменение свойств элементов: в начале периода (кроме первого) находится щелочной металл, затем наблюдается постепенное ослабление металлических свойств и усиление неметаллических. Эта закономерность прослеживается для элементов второго периода в таблице 4.2.
Таблица 4.2.

В больших периодах с ростом заряда ядер заполнение уровней электронами происходит сложнее, что и объясняет более сложное изменение свойств элементов по сравнению с элементами малых периодов.
Одинаковый характер свойств химических элементов в подгруппах объясняется сходным строением внешнего энергетического уровня, как это показано в табл. 4.3, иллюстрирующей последовательность заполнения электронами энергетических уровней для подгрупп щелочных металлов.
Таблица 4.3.

Номер группы, как правило, указывает на число электронов в атоме, которые могут участвовать в образовании химических связей. В этом заключается физический смысл номера группы. В четырех местах периодической системы элементы расположены не в порядке возрастания атомных масс: Ar и K, Co и Ni, Te и I, Th и Pa . Эти отступления считались недостатками периодической системы химических элементов. Учение о строении атома объяснило указанные отступления. Опытное определение зарядов ядер показало, что расположение этих элементов соответствует возрастанию зарядов их ядер. Кроме того, опытное определение зарядов ядер атомов дало возможность определить число элементов между водородом и ураном, а также число лантаноидов. Ныне все места в периодической системе заполнены в промежутке от Z=1 до Z=114, однако периодическая система не закончена, возможно открытие новых трансурановых элементов.
Структура химических систем
Характер любой системы зависит не только от состава и строения ее элементов, но и от их взаимодействия. Совокупность тех специфических взаимосвязей и взаимодействий, благодаря которым возникают новые целостные свойства, присущие только системе и отсутствующие у отдельных ее компонентов, называются структурой системы. Поэтому при исследовании разнообразных веществ и их реакционной способности ученым химикам приходилось заниматься и изучением их структур. В качестве первичной химической системы рассматривалась при этом молекула и поэтому под структурой вещества, прежде всего, понималась структура молекулы, как наименьшей частицы вещества.
Представления о структуре молекулы по мере развития химической науки постепенно совершенствовались, уточнялись, конкретизировались, начиная от весьма общих положений отвлеченного характера, и кончая гипотезами, обоснованными с помощью систематических химических экспериментов.
Так, известный шведский химик Й. Берцелиус (1779–1848), французский химик Ш. Жерар (1815–1856), немецкий химик Ф. Кекуле (1839–1866) пытались в своих теориях ответить на вопрос: существует ли какая либо упорядоченность в объединении атомов в молекуле или они объединяются произвольно.
На этой основе их разработок возникли структурные формулы, в которых элементы связывались друг с другом по числу их валентности. Комбинируя атомы по их валентности можно было прогнозировать получение различных соединений в зависимости от исходных реагентов. Таким путем можно было уже управлять процессом синтеза веществ с различными свойствами.
Последнее изменение этой страницы: 2016-07-23
lectmania.ru. Все права принадлежат авторам данных материалов. В случае нарушения авторского права напишите нам сюда...