
Категории:
ДомЗдоровьеЗоологияИнформатикаИскусствоИскусствоКомпьютерыКулинарияМаркетингМатематикаМедицинаМенеджментОбразованиеПедагогикаПитомцыПрограммированиеПроизводствоПромышленностьПсихологияРазноеРелигияСоциологияСпортСтатистикаТранспортФизикаФилософияФинансыХимияХоббиЭкологияЭкономикаЭлектроника
Ионно - молекулярные реакции обмена
Провести реакции между растворами электролитов согласно заданию. Для этого в пробирку налить 7 ─ 8 капель одного реактива и добавить 7 ─ 8 капель другого реактива. Отметить признаки реакции: выпадение осадка, выделение газа или изменение запаха (что свидетельствует об образовании малодиссоциирующего вещества).
Затем, в соответствии с наблюдаемыми признаками, отнести реакцию к одному из 3-х типов:
1) ионообменные реакции с образованием малорастворимого вещества (осадка);
2) ионообменные реакции с выделением газа;
3) ионообменные реакции с образованием слабого электролита.
Каждую реакцию записать в 3-х формах:
а) молекулярной,
б) полной ионно-молекулярной,
в) сокращенной ионно-молекулярной.
Сделайте вывод о направлении протекания реакций ионного обмена.
Задания для опытов
| 1. CH3COONa+H2SO4 2. NaNO2+ H2SO4 3. MgCl2+Na3PO4 4. NH4Cl+KOH 5. Na2CO3+HCl 6. Na2CO3+Ba(NO3)2 7. (CH3COO)2Pb+HCl 8. Hg(NO3)2+NaOH 9. H2SO4+BaCl2 10. NaCl+Pb(NO3)2 11. NiSO4+KOH 12. NaNO2+HCl 13. Bi(NO3)3+KOH 14. Na2S+CdCl2 15. Bi(NO3)3+Na2S 16. CoSO4+KOH 17. CuSO4+KOH 18. Na2CO3+HNO3 19. K2CrO4+ CuSO4 20. K2CrO4+ MnSO4 21. K2CrO4+ NiSO4 22. K2CO3+ MnSO4 23. Na2SO3+HCl | 24. Hg(NO3)2+Na2S 25. NiSO4+ NH4OH 26. NiSO4+ NH4OHизб 27.AlCl3+KOH 28. FeCl3+Na3PO4 29. K2CrO4+ Ba(NO3)2 30. NaNO2+HNO3 31. MgCl2+ NaOH 32. CuSO4+ NH4OH 33. CuSO4+ NH4OHизб 34. AlCl3+KOHизб 35. Pb(NO3)2+KI 36. CH3COOK+ HCl 37. Al2(SO4)3+NaOH 38. Al2(SO4)3+NaOHизб 39. CoSO4+ Na2S 40. Pb(NO3)2+ Na3PO4 41. Na3PO4+ CuSO4 42. CH3COOK+ HNO3 43. CH3COOH+KOH 44. CoSO4+ NH4OH 45. CoSO4+ NH4OHизб 46. Hg(NO3)2+ KI | 47. Hg(NO3)2+ KIизб 48. CdCl2+ NH4OH 49. CdCl2+ NH4OHизб 50. NaHCO3+ HNO3 51. ZnSO4+ BaCl2 52. ZnSO4+KOH 53. ZnSO4+KOHизб 54. (CH3COO)2Pb+ H2SO4 55. NaHCO3+H2SO4 56. (NH4)2SO4+KOH 57. K2CO3+ H2SO4 58. (NH4)2SO4+NaOH 59. K2CO3+ HCl 60. CrCl3+KOH 61. CrCl3+KOHизб 62. ZnCl2+NaOH 63. ZnCl2+NaOHизб 64. MnSO4+KOH 65. MnSO4+Na3PO4 66. Na2SO3+ H2SO4 67. K2CO3+ CH3COOH 68. Na2CO3+CH3COOH 69. NaHCO3+CH3COOH |
Лабораторная работа №6
ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ. ГИДРОЛИЗ СОЛЕЙ
Цель работы: определить рН растворов и реакцию среды, изучить различные случаи гидролиза солей.
Теоретическая часть
1. Водородный показатель рН
Многие реакции, которые протекают в водных растворах электролитов, объясняются тем, что вода в очень малой степени диссоциирует на ионы по уравнению:
 .
.
Обратимый процесс по закону действия масс характеризуется константой диссоциации:
 .
.
Так как степень диссоциации воды очень мала (  ), то концентрацию молекул воды можно считать постоянной величиной. Тогда
), то концентрацию молекул воды можно считать постоянной величиной. Тогда
 .
.
 называется ионным произведением воды, его величина при 25 0С равна 1,008·10-14, если концентрации ионов Н+ и ОН- выражены в моль/л:
называется ионным произведением воды, его величина при 25 0С равна 1,008·10-14, если концентрации ионов Н+ и ОН- выражены в моль/л:

 .
.
В чистой воде и в любой нейтральной среде 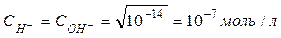 .
.
В кислых растворах концентрация ионов водорода больше концентрации гидроксид-ионов
 >
>  ;
;  <
<  .
.
В щелочных растворах концентрация гидроксид-ионов больше, чем концентрация ионов водорода:
 <
< 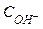 ;
;  >
> 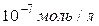 .
.
Практически более удобно реакцию раствора характеризовать водородным показателем рН:
 .
.
В нейтральной среде рН = 7, кислой среде рН < 7 , щелочной среде рН > 7.
Водородный показатель количественно характеризует реакцию среды. Любой химико-технологический процесс оптимально протекает только при определенном рН. Например, водородный показатель питьевой воды должен быть в пределах 6 ... 9.
Гидролиз солей
Кроме оснований и кислот, растворы которых имеют кислую или щелочную среду, растворы солей имеют также кислую или щелочную среду, реже ─ нейтральную.
Причиной изменения рН раствора являются обменные реакции взаимодействия ионов солей с молекулами воды, называемые реакциями гидролиза.
Процесс гидролиза является обратимым. В растворе соли, подвергшейся гидролизу, устанавливается равновесие между солью и продуктами гидролиза:
KtAn + H2O  KtOH + HAn,
KtOH + HAn,
количественно характеризующееся константой гидролиза:
 .
.
Тип реакции гидролиза и соответственно характер среды водных растворов солей зависит от химической природы катионов и анионов, образующих соли. Гидролизу подвергается не вся соль в растворе. Отношение числа гидролизованных молекул соли к общему числу растворенных молекул называется степенью гидролизаh. Чем слабее кислота (или основание), тем больше степень гидролиза ее соли. Константа и степень гидролиза связаны между собой соотношением:
 .
.
Из данного выражения следует, что при уменьшении концентрации соли (при разбавлении раствора) степень гидролиза соли увеличивается, т. е. равновесие реакции гидролиза смещается в сторону образования продуктов гидролиза.
Реакция гидролиза протекает с поглощением теплоты (эндотермическая реакция). Поэтому при повышении температуры, по принципу Ле Шателье,равновесие реакции гидролиза смещается в сторону продуктов гидролиза, т. е. степень гидролиза соли увеличивается.
Итак, для уменьшения степени гидролиза растворы солей следует хранить концентрированными и при низких температурах.
Гидролиз имеет большое значение. Разрушение горных пород обусловлено в значительной мере гидролизом составляющих их минералов – алюмосиликатов. Твердение вяжущих веществ, осахаривание крахмала, гидролиз древесины, получение мыла и много других важных производств основано на гидролизе.
Различают три случая обратимого гидролиза солей: катионный, анионный и катионно-анионный. Такая классификация реакций гидролиза дается по тому иону соли, который связывает ионы Н+ или ОН- в слабый электролит: кислоту, гидроокись, кислый анион, основной катион.
Катионный гидролиз.Этому виду гидролиза подвергаются соли, образованные слабым основанием и сильной кислотой, например: CuSO4, FeCl3, NH4Cl, Zn(NO3)2, MnBr2 и др. Гидролиз такого типа солей обусловлен связыванием катионов слабых гидроксидов (Cu2+, Fe3+, NH4+, Zn2+, Mn2+)с гидроксид-ионами воды и образованием слабого основания в случае катиона одновалентного металла и основной соли в случае катиона многовалентного металла.
Например, гидролиз соли MnBr2, образованной слабым основанием и сильной кислотой, происходит в 2 стадии. При комнатной температуре гидролиз идет преимущественно по I ступени. Сокращенное ионно-молекулярное уравнение I ступени, отражающее суть реакции, выглядит следующим образом:
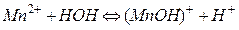 .
.
Из уравнения следует, что при гидролизе солей по катионному типу в растворе накапливаются ионы Н+, поэтому среда становится кислой (рН < 7).
Значение константы гидролиза можно рассчитать либо на основании равновесных концентраций участников реакции гидролиза:
 ,
,
либо используя табличные значения константы соответствующего этапа диссоциации слабого основания:
 .
.
Полное ионно-молекулярное уравнение катионного гидролиза получается добавлением в обе части сокращенного ионно-молекулярного уравнения анионов сильной кислоты:
 .
.
Молекулярное уравнение получают, объединяя ионы в молекулы:
 .
.
Таким образом, на первом этапе гидролиза образуется основная соль MnOHBr.
При нагревании и разбавлении раствора гидролиз усиливается и протекает вторая ступень гидролиза. Сокращенное ионно-молекулярное уравнение II ступени имеет вид:
 ,
, 
 ;
;
полное ионно-молекулярное уравнение: 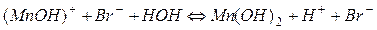 ,
,
и молекулярная форма II ступени:  .
.
Анионный гидролиз.Анионному гидролизу подвергаются соли, образованные сильным основанием и слабой кислотой, например: Li2CO3, К3РО4, Ва(СН3СОО)2, CaS, Na2B4O7. Гидролиз этого типа солей обусловлен связыванием анионов слабых кислот (  ) с катионом Н+ воды с образованием слабой кислоты в случае, если анион соли одновалентен, и кислой соли, если анион соли многовалентен.
) с катионом Н+ воды с образованием слабой кислоты в случае, если анион соли одновалентен, и кислой соли, если анион соли многовалентен.
Например, гидролиз соли Li2CO3, образованной сильным основанием и слабой кислотой, происходит в 2 стадии. При комнатной температуре гидролиз идет преимущественно по I ступени. Сокращенное ионно-молекулярное уравнение I ступени, отражающее суть реакции, выглядит следующим образом:
 .
.
Из уравнения следует, что при гидролизе солей по анионному типу в растворе накапливаются ионы ОН-, поэтому среда становится щелочной (рН > 7).
Значение константы гидролиза можно рассчитать либо на основании равновесных концентраций участников реакции гидролиза:
 ,
,
либо используя табличные значения константы соответствующего этапа диссоциации слабой кислоты:
 .
.
Полное ионно-молекулярное уравнение анионного гидролиза получается добавлением в обе части сокращенного ионно-молекулярного уравнения катионов сильного основания:
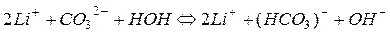 .
.
Молекулярное уравнение получают, объединяя ионы в молекулы:
 .
.
Таким образом, на первом этапе гидролиза образуется кислая соль LiHCO3.
При нагревании и разбавлении раствора гидролиз усиливается и протекает вторая ступень гидролиза. Сокращенное ионно-молекулярное уравнение II ступени имеет вид:
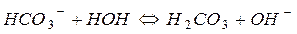 ,
, 
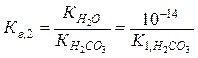 ;
;
полное ионно-молекулярное уравнение:  ,
,
и молекулярная форма 2-й ступени:  .
.
Катионно-анионный гидролиз.Катионно-анионному гидролизу подвергаются соли, образованные слабым основанием и слабой кислотой, например: Fе(CH3COO)2, (NH4)2SO4, NH4CN, CH3COONH4.
Гидролиз данного типа протекает в результате связывания катионов соли с ионами ОН- и анионов соли с ионами Н+ воды с образованием слабых электролитов. Например, для соли CH3COONH4:
СН3СОО- + NН4+ + Н2О  СН3СООН + NH4ОН,
СН3СООН + NH4ОН,
или в молекулярной форме:
СН3СООNН4 + Н2O  СH3СООН + NH4OH;
СH3СООН + NH4OH;
рН среды в таких растворах зависит от относительной силы образующихся слабой кислоты и слабого основания. В данной реакции рН = 7, так как константы диссоциации CH3COOH и NH4OH равны. Если соли образованы очень слабыми гидроксидами и очень слабыми кислотами, то они гидролизуются необратимо и продукты гидролиза их выходят из сферы реакции в виде осадка, газа или слабодиссоциирующего вещества, например:
Сr2S3 + 6Н2О = 2Сr(ОН)3↓ +3H2S.
Соли, не подвергающиеся гидролизу.Соли, образованные сильным основанием и сильной кислотой, гидролизу не подвергаются, так как ни один из ионов такой соли не связывается с ионами воды в слабый электролит. Примеры таких солей: KNO3, Na2SO4, CaCl2, NaI и т. д.
Водные растворы таких солей имеют нейтральную среду, рН = 7.
Практическая часть
Опыты №1,2,3 выполняются следующим образом: на полоску универсальной индикаторной бумаги нанести несколько капель раствора, а затем сравнить окраску бумаги со шкалой. Оформить опыты, выбрав подходящее название для 2 и 3 опыта.
Опыт №1. Индикаторный метод определения рН растворов
Измерить значения рН растворов кислот и оснований, а также 2-х солей, указанных преподавателем, результаты занести в табл.6.1. На основании измеренных значений рН рассчитать для каждого из растворов концентрации ионов Н+ и ОН-, а также указать реакцию среды (кислая, нейтральная или щелочная). Расчетные формулы и пример расчета для одного из растворов привести после таблицы.
Таблица 6.1. Значения рН водных растворов электролитов
| Название растворов | рН растворов |  ,
моль/л ,
моль/л
|  ,
моль/л ,
моль/л
| Реакция среды |
| 1. Дист. вода 2. СН3СООН 3.HCl 4. NH4OH 5. NaOH 6. 7. |
Опыт №2. Гидролиз соли, образованной сильным основанием и слабой кислотой
По характеру среды водного раствора выбрать соль, относящуюся к данному типу. Написать уравнение гидролиза соли в молекулярной и ионно-молекулярных формах.
На основании измеренного значения рН данной соли и табличного значения константы диссоциации слабой кислоты рассчитать константу и степень гидролиза данной соли.
Опыт №3. Гидролиз соли, образованной слабым основанием и сильной кислотой
По характеру среды водного раствора выбрать соль, относящуюся к данному типу. Написать уравнение гидролиза соли в молекулярной и ионно-молекулярных формах.
На основании измеренного значения рН данной соли и табличного значения константы диссоциации слабого основания рассчитать константу и степень гидролиза данной соли.
Опыт №4. Влияние разбавления на степень гидролиза
Разбавить исходный 0,1М раствор одной из солей водой в 10 раз с помощью мерного цилиндра, измерить рН полученного раствора и сравнить его с измеренным ранее рН соли до разбавления. Сделать вывод о влиянии разбавления на степень гидролиза.
Опыт №5. Влияние нагревания на степень гидролиза
Раствор одной из солей налить в микропробирку и нагреть до 50 – 60 0С путем помещения на водяную баню. Измерить рН нагретого раствора соли и сравнить его с измеренным ранее рН соли при комнатной температуре. Сделать вывод о влиянии температуры на степень гидролиза.
Лабораторная работа №7
Последнее изменение этой страницы: 2016-08-11
lectmania.ru. Все права принадлежат авторам данных материалов. В случае нарушения авторского права напишите нам сюда...