
Категории:
ДомЗдоровьеЗоологияИнформатикаИскусствоИскусствоКомпьютерыКулинарияМаркетингМатематикаМедицинаМенеджментОбразованиеПедагогикаПитомцыПрограммированиеПроизводствоПромышленностьПсихологияРазноеРелигияСоциологияСпортСтатистикаТранспортФизикаФилософияФинансыХимияХоббиЭкологияЭкономикаЭлектроника
ОСНОВНЫЕ КЛАССЫ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ И ИХ РЕАКЦИОННАЯ СПОСОБНОСТЬ
О.А. Журавская
ОСНОВНЫЕ КЛАССЫ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ И ИХ РЕАКЦИОННАЯ СПОСОБНОСТЬ
Учебно-методическое пособие
для студентов медицинских вузов
Самара 2011
УДК
Ж 91
Рецензенты:
– кандидат химических наук, доцент А.А. Данилин;
– кандидат химических наук, доцент О.К. Шаховкина.
Журавская О.А. Основные классы органических соединений и их реакционная способность:Учебно-методическое пособие для студентов медицинских вузов. – Самара, НОУ ВПО «Самарский медицинский институт «РеаВиЗ», 2011 − 52 с. ???
Изучение биоорганической химии в медицинских вузах связано с усвоением большого объема материала при малом количестве аудиторных часов.
В учебном пособии освещены вопросы строения и реакционной способности основных классов органических соединений, материал представлен в текстуальной форме, таблицах, схемах и рисунках, что позволяет оптимизировать процесс запоминания.
Пособие предназначено для студентов медицинских вузов, обучающихся по специальностям «Лечебное дело» и «Стоматология» очной и очно-заочной формы обучения.
© НОУ ВПО СМИ «РеаВиЗ», 2011
Раздел 2. Основные классы органических соединений и их реакционная способность
Реакционная способность алифатических и ароматических углеводородов
Реакционная способность алканов и циклоалканов
К предельным (или насыщенным) углеводородам относят углеводороды, в молекулах которых атомы углерода находятся в состоянии sp3-гибридизации. По строению углеродного скелета такие углеводороды делят на алканы и циклоалканы.
Алканы – это ациклические насыщенные углеводороды с общей формулой СnH2n+2.
Неполярные связи С–С и С–Н в алканах (и циклоалканах) не склонны к ионному разрыву, но способны расщепляться гомолитически под действием свободных радикалов.
Значит, для алканов характерны реакции радикального замещения SR (от англ. substitution radicalic).
По этому механизму протекают реакции галогенирования (алканы циклоалканы С5 – С6):
Этапы:
1. Инициирование цепи:

свободные радикалы
Высокая реакционная способность радикалов объясняется их стремлением достроить внешний электронный уровень до устойчивого октета.
2. Развитие цепи:


В результате последовательных реакций в цепи могут образоваться:
CH3Cl – хлористый метил (хлорметан);
CH2Cl2 – хлористый метилен (дихлорметан);
CHCl3 – хлороформ (трихлорметан);
CCl4 – четыреххлористый углерод (тетрахлорметан).
3. Обрыв цепи:
а) Cl· + Cl· → Cl2
б) CH3· + Cl· → CH3Cl
в) CH3· + CH3· → CH3 – CH3
Реакция региоселективна.
Региоселективность – предпочтительное протекание реакции по одному из нескольких реакционных центров одинаковой химической природы.
Скорость SR:
третичные УВ > вторичные УВ > первичные УВ
(связано со стабильностью образующихся радикалов и подвижностью водородов под влиянием +J-эффекта)
Медико-биологическое значение насыщенных углеводородов
· смесь аканов до С15 – вазелиновое масло;
до С25 – вазелин – основа мазей;
до С35 – парафин – парафинолечение.
Реакционная способность непредельных углеводородов
К ненасыщенным (непредельным) относятся такие углеводороды, которые могут быть насыщены атомами водорода. Они могут содержать одну или несколько двойных связей, тройных связей, или их комбинации.
| Непредельные (ненасыщенные) углеводороды | |||
алкены
 этилен
этилен
| циклоалкены
 циклопентен
циклопентен
| алкадиены
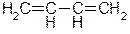 бутадиен-1,3
бутадиен-1,3
| акины
 этин
этин
|
Типичные реакции ненасыщенных соединений - АЕ (от англ. Addition electrophilic)

Механизм реакций АЕ

Схема механизма реакции гидратации

Медико-биологическое значение непредельных углеводородов
· диеновые углеводороды – основа натуральных и синтетических каучуков – изготовление изделий медицинского и санитарно-гигиенического назначения.
Примеры реакций электрофильного замещения

Роль катализатора:

Биологическая роль реакций SE – биосинтез гормонов щитовидной железы (пример реакции SE in vivo).

Механизм реакций SE в ароматическом кольце

1. Генерирование электрофильной частицы

2. Образование π-комплекса

3. Образование σ-комплекса

4. Образование конечного продукта (стабилизация σ-комплекса)

Однозамещенные бензола изомеров не имеют, но если в кольце появляются заместители, то симметрия кольца нарушается и с помощью квантово-механических расчетов удалось установить, что все заместители делят на 2 группы: электронодоноры и электроноакцепторы.
Окисление

Восстановление

Присоединение хлора

Антрацена и фенантрена
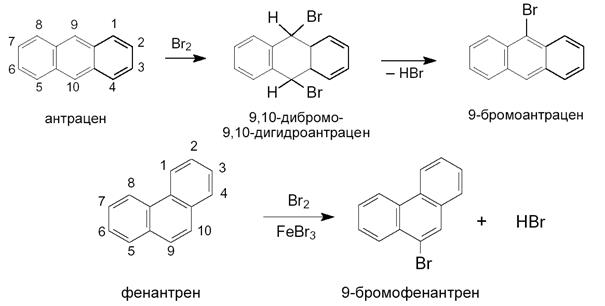
Антрацен более реакционноспособен по сравнению с фенантреном.
Спирты и фенолы
Производные алифатических углеводородов, в которых один или несколько атомов водорода замещены на гидроксильную группу, называют спиртами; аналогичные производные моноядерных ароматических углеводородов называют фенолами; производные нафталина – нафтолами.
Различают:
- по числу групп – ОН:
· одноатомные;
· многоатомные спирты и фенолы;
- по типу атома углерода, соединенному с группой –ОН:
· первичные

· вторичные

· третичные

Простые эфиры– это производные спиртов и фенолов, в которых атом водорода группы – ОН замещен алкильным (R-) или арильным (Ar-) радикалом (R – O – R' или R – O – Ar).
Эпоксиды Пероксиды

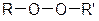
Виниловые эфиры Гидропероксиды


Простые эфиры с водой не смешиваются, хорошо растворяют многие органические вещества, весьма огнеопасны.
Свойства спиртов и фенолов.
Связь С – О в спиртах и фенолах полярна и способна к гетеролитическому разрыву.
- взаимодействуют с галогеноводородными кислотами:

- нейтральный характер спиртов и слабые кислотные свойства фенолов:



- образуют простые и сложные эфиры:


Фенолов, простых эфиров
· Введение ОН-группы повышает растворимость вещества в воде и увеличивает его физиологическую активность.
- Метанол CH3OH – сильный яд.
- Этанол CH3CH2OH – антисептическое средство, используется в качестве обеззараживающего средства и для приготовления настоек.
- Бутиловые и амиловые спирты – основные компоненты сивушных масел.
· Введение ОН-группы в ароматическое ядро приводит к появлению антисептических свойств.
- Фенол (карболовая кислота) – применяется как дезинфицирующее средство (первый антисептик, введенный в хирургию).
- Крезолы (смесь 2-, 3- и 4-метилфенолов) – применяются как дезинфицирующие средства.
- Диэтиловый эфир (C2H5)2O – средство для ингаляционного наркоза, используется для приготовления настоек и экстрактов; при хранении на воздухе образует взрывчатый гидропероксид.
- Эпоксиды предполагаются в качестве промежуточных продуктов при ферментативном окислении кислородом связей С=С.
- Бутилвиниловый эфир CH2=CH–O–C4H9

используется для получения полимера, применяемого как ранозаживляющее средство («бальзам Шостаковского»).
Тиолы и амины
Серосодержащие аналоги спиртов (или фенолов) называют тиолами (или тиофенолами), серосодержащие аналоги простых эфиров и органических пероксидов называют сульфидамиидисульфидами:
R – SH Ar – SH R – S – R R – S – S – R
Атома углерода
Многие биологически активные органические веществ: белки, жиры, углеводы, гормоны и другие, содержат в своем составе углерод-кислородную двойную связь, называемую карбонильной группой (или оксогруппой).
Альдегидами называют соединения, в которых карбонильная группа соединена с углеводородным радикалом и атомом водорода; общая формула:
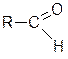
Кетоны– содержат карбонильную группу, связанную с двумя углеводородными радикалами:

Различают:
· В зависимости от строения углеводородного радикала:
| алифатические | алициклические | ароматические |
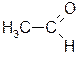 этаналь
(ацетальдегид)
этаналь
(ацетальдегид)
 пропанон (ацетон)
пропанон (ацетон)
| 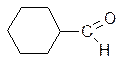 циклогексанкарбальдегид
циклогексанкарбальдегид
 циклогексанон
циклогексанон
| 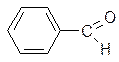 бензальдегид
бензальдегид
 бензофенон
бензофенон
|
Карбонильной группы
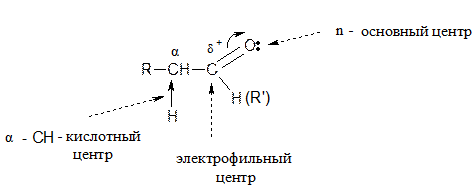
· Электрофильный центр – карбонильный атом углерода, на котором возникновение частичного положительного заряда обусловлено полярностью связи C=O (реакции AN).
· Основный центр – атом кислорода с неподеленными парами электронов (кислотный катализ в реакциях присоединения).
· α – СН – кислотный центр возникает за счет индуктивного эффекта карбонильной группы (реакции конденсации).

Трихлоруксусный
Альдегид (хлораль)
Галогены обладают (-)I – эффектом.
2 стадия: непрочное соединение – трихлоруксусный альдегид легко расщепляется под действием NaOH, так как оба его углерода несут частичные положительные заряды (δ+)

Галоформная реакция используется как способ получения карбоновых кислот и для обнаружения метилкетонов (ацетона) и ацетальдегида – йодоформная проба – в биологических жидкостях.
· Реакции присоединения – отщепления AN – E (образование оснований Шиффа):
1 стадия: нуклеофильная атака аминами карбонильного атома углерода

2 стадия: стабилизация биполярного иона

3 стадия: отщепление (элиминирование) с образованием основания Шиффа

В организме образование оснований Шиффа идет при биосинтезе аминокислот из кетокислот и при распаде аминокислот через стадию переаминирования.
У тригонального атома углерода
Карбоновыми кислотаминазывают соединения, содержащие карбоксильную группу – СООН.
Различают:

Карбоксильная группа:

образуется за счет карбонильной группы и гидроксильной. Свойства карбоксильной группы не равны сумме свойств карбонильной и гидроксильной групп, это новая функциональная группа, обладающая собственными свойствами:

- по данным рентгеноструктурного анализа в карбоксилат-ионе нет на двойной, ни одинарной связи – связь полуторная;
- выравненность электронной плотности происходит вследствие делокализации электронов, образуется сопряженная трехцентровая система;
- в результате такого электронного строения карбоксилат-иона уменьшается δ+ на атоме углерода и для карбоксильной группы не характерны реакции AN, а свойственны реакции SN.
Механизм реакции этерификации
1 стадия: образование карбокатиона I под влиянием протона (Н+) катализатора. Роль катализатора – повышение положительного заряда на углероде карбоксильной группы.

2 стадия: нуклеофильная атака карбокатиона I молекулой спирта с образованием комплексного иона II

3 стадия: образовавшийся комплексный ион II неустойчив, так как легко теряет Н2О: а) реакция сдвигается в сторону образования Н2О (среда – безводная, контроль – кинетический); б) с другой стороны, Н2О – более термодинамически устойчивая молекула (контроль - термодинамический); образуется карбокатион III

4 стадия: стабилизация карбокатиона III выбросом протона (Н+) с образованием сложного эфира

Реакция этерификации обратима, если добавить большие количества Н2О, то реакция сдвигается в сторону гидролиза сложных эфиров с образованием карбоновых кислот и спиртов. Скорость реакции этерификации зависит от строения карбоновых кислот и спиртов: при одной и той же карбоновой кислоте скорость этерификации первичных спиртов в 2 раза выше, чем вторичных и во много раз выше, чем третичных, что зависит от пространственного расположения радикалов («пространственные затруднения»).
Гидролиз сложных эфиров может проходить как в кислой, так и в щелочной среде. Причем гидролиз в щелочной среде (омыление) необратим и идет в 1000 раз быстрее кислотного (причина – щелочь – реагент, а не катализатор):


Галогенангидридами карбоновых кислот называют продукты замещения группы –ОН в –СООН на атом галогена:
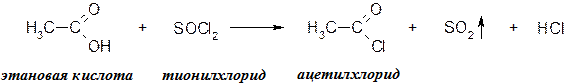
Ангидридами карбоновых кислот называют продукты отщепления молекулы воды от двух молекул монокарбоновых кислот (или одной молекулы дикарбоновой кислоты):
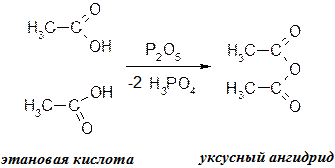
Более универсальный способ:

Амидами карбоновых кислот называют продукты замещения группы –ОН в –СООН на аминогруппу (или на замещенную аминогруппу):


Функциональные производные карбоновых кислот – обладают ацилирующей способностью, которая уменьшается в ряду:

· Реакции за счет углеводородного радикала:
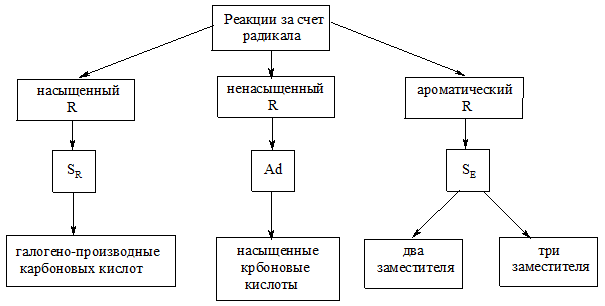

· Реакции декарбоксилирования (протекают тем с большей скоростью, чем ближе друг к другу находятся группы –СООН):
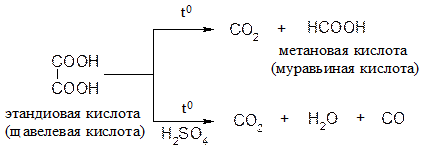
И их производных
· Входят в состав простых и сложных липидов;
· Функциональные производные карбоновых кислот – основа лекарственных препаратов, дезинфицирующих средств, консервантов. (Бензоат натрия C6H5COONa – отхаркивающее средство; метилизовалериат C4H9COOCH3 – основа валидола)
Двухатомные фенолы

Пирокатехин (о-дигидроксибензол, катехол) – структурный фрагмент многих БАВ, в частности, катехоламинов.
Резорцин (м-дигидроксибензол) – обладает антисептическим действием, применяется в мазях, примочках при экземе.
Многоосновные гидроксикислоты

Аминотиолы
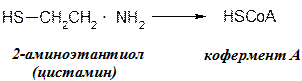
Цистамин – радиопротектор. Повышает устойчивость организма к воздействию ионизирующей радиации. Действие основано на способности уменьшать число радикалов, ионизированных и возбужденных молекул, образующихся в тканях.
Гидроксикарбонильные соединения(гидроксиальдегиды и гидроксикетоны)


Важные метаболиты – продукты распада глюкозы при гликолизе, исходные соединения при биосинтезе моносахаридов.
Альдегидо- и кетонокислоты

Многоосновные кетонокислоты

Обе кислоты – участники цикла Кребса, щавелевоянтарная кислота, кроме того, является связующим звеном между метаболизмом углеводов и аминокислот.
Аминосульфокислоты

Таурин участвует в синтезе ряда аминокислот и энергетическом обмене в мышечных тканях, входит в состав желчных кислот, способствующих эмульгированию жиров в кишечнике. Необходим для поддержания нормального уровня холестерина в крови; предотвращает выведение калия из сердечной мышцы.
Тетрапиррольные соединения



Индол и его производные



Будучи похожими по своей химической структуре, они замещают серотонин в мозгу и нервной системе и извращают его действие. Организм такого обмена не прощает, и серотониновая система, контролирующая в нем большинство жизненно важных процессов, таких как память, поведение, интеллект и многие другие, начинает работать со сбоями, что, в конечном итоге, заканчивается психозом и полной деградацией личности.

Диэтиламид эргометрин
Лизергиновой
Кислоты
Эргометрин — лекарственный препарат, повышающий тонус мышц матки и применяющийся для остановки маточных кровотечений и для ускорения обратного развития матки в послеродовом периоде. Длительное
применение этого препарата может привести к хроническому отравлению (эрготизму) выражающемуся либо в некрозе тканей, в особенности конечностей (антонов огонь) или в судорогах или конвульсиях (злая корча).
Хинолин и его производные

Пиридиновое кольцо более устойчиво к окислению, но легче гидрируется.

Обладает бактерицидным действием.

Таутомерия пиразолонов

Обезболивающее, жаропонижающее и противовоспалительное действие. Ненаркотические анальгетики.
Библиографический список
1. Грандберг И. И. Органическая химия: учебник для студентов, обучающихся по агрохимическим специальностям. – М.: Дрофа, 2002. - 672 с.
2. Зурабян С. Е. Основы органической химии. М.: Дрофа, 2006. - 576 с.
3. Оганесян Э. Т. Важнейшие понятия и термины химии: справочное пособие. – М.: Высшая школа, 1993. - 352 с.
4. Проскурина И. К. Биохимия: учебное пособие для студентов высших учебных заведений. – М.: Издательство Владос-Пресс, 2004. - 70 с.
5. Солдатенков А. Т. Основы органической химии лекарственных веществ. М.: Мир; БИНОМ. Лаборатория занятий, 2007. - 191 с.
6. Сорочинская Е. И. Биоорганическая химия. Поли- и гетерофункциональные соединения. Биополимеры и их структурные компоненты. Учебное пособие. – СПб.: Издательство С.Петербургского университета, 1998. - 148 с.
7. Сорочинская Е. И. Биоорганическая химия. Биологически важные классы соединений. Учебное пособие. – СПб: Издательство С.Петербургского университета. - 1998.
8. Тюкавкина Н. А. Биоорганическая химия: учебник для вузов. – М.: Дрофа, 2005. – 542 с.
9. Тюкавкина Н. А. Органическая химия. – м.: Дрофа, 2003. – Кн.1: Основной курс. – 640 с.
О.А. Журавская
ОСНОВНЫЕ КЛАССЫ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ И ИХ РЕАКЦИОННАЯ СПОСОБНОСТЬ
Учебно-методическое пособие
для студентов медицинских вузов
Самара 2011
УДК
Ж 91
Рецензенты:
– кандидат химических наук, доцент А.А. Данилин;
– кандидат химических наук, доцент О.К. Шаховкина.
Журавская О.А. Основные классы органических соединений и их реакционная способность:Учебно-методическое пособие для студентов медицинских вузов. – Самара, НОУ ВПО «Самарский медицинский институт «РеаВиЗ», 2011 − 52 с. ???
Изучение биоорганической химии в медицинских вузах связано с усвоением большого объема материала при малом количестве аудиторных часов.
В учебном пособии освещены вопросы строения и реакционной способности основных классов органических соединений, материал представлен в текстуальной форме, таблицах, схемах и рисунках, что позволяет оптимизировать процесс запоминания.
Пособие предназначено для студентов медицинских вузов, обучающихся по специальностям «Лечебное дело» и «Стоматология» очной и очно-заочной формы обучения.
© НОУ ВПО СМИ «РеаВиЗ», 2011
Последнее изменение этой страницы: 2016-08-11
lectmania.ru. Все права принадлежат авторам данных материалов. В случае нарушения авторского права напишите нам сюда...