
Категории:
ДомЗдоровьеЗоологияИнформатикаИскусствоИскусствоКомпьютерыКулинарияМаркетингМатематикаМедицинаМенеджментОбразованиеПедагогикаПитомцыПрограммированиеПроизводствоПромышленностьПсихологияРазноеРелигияСоциологияСпортСтатистикаТранспортФизикаФилософияФинансыХимияХоббиЭкологияЭкономикаЭлектроника
Адсорбция на границе жидкость – газ
Адсорбция приводит к изменению поверхностного натяжения жидкости s. Вещества, снижающие в результате адсорбции поверхностное натяжение жидкости, называются поверхностно – активными (ПАВ). Вещества, поверхностное натяжение растворов которых по отношению к растворителю увеличивается, называются поверхностно – инактивными(ПИВ).
Способность вещества при адсорбции на границе раздела фаз снижать поверхностное межфазовое натяжение в зависимости от его концентрации в объеме называют поверхностной активностью.Поверхностная активность равна:
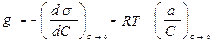 .
.
В случае адсорбции ПАВ g > 0 и (ds / dC) < 0.
Снижение поверхностного натяжения Ds в результате адсорбции ПАВ на границе раздела жидкость – газ можно определить при помощи уравнения Шишковского:
 , (26)
, (26)
где A, B – эмпирические коэффициенты.
Пример 20. При Т =298 К поверхностное натяжение (σ) воды равно 72,75 мДж / м2
Для 0,05 М раствора уксусной кислоты поверхностное натяжение равно 71, 2 мДж / м2. Рассчитать адсорбцию уксусной кислоты на поверхности раствора.
Решение. Воспользуемся уравнением Гиббса:
 .
.
Заменим производную dσ / dC отношением Δσ / ΔC , так как по условию дано только два значения поверхностного натяжения. Тогда:
g = - (Δ σ / Δ С ) = - (71,2 – 72,75) . 10 – 3 / 0,05 . 10 3 = 31. 10 – 6 (Дж . м) / моль
После подстановки в уравнение Гиббса получим:
a = 0,05 . 10 3 · 31· 10 - 6 / 8,314· 298 = 0,626· 10 - 6 моль / м 2
Пример 21. По приведенным результатам исследования адсорбции пропана на активном угле, проведенного при 20 0С, составьте уравнение изотермы адсорбции Ленгмюра и определите удельную поверхность угля. Площадь сечения молекул пропана принять равной
1,86 . 10 – 19 м 2.
| p (С3Н8), Торр | 1,0 | 10,0 | 50,0 | |||
| a, моль/кг | 0,086 | 0,673 | 1,705 | 2,045 | 2,568 | 2,617 |
Решение. Воспользуемся линейной формой уравнения Ленгмюра в виде:
 .
.
Составляем вспомогательную таблицу
| p , Торр | 1,0 | 10,0 | 50,0 | |||
| p / a, Торр . моль – 1 . кг | 11,628 | 14,859 | 29,326 | 48,900 | 155,763 | 267,482 |
Данные таблицы представим в виде графика p / a = f (p). Угловой коэффициент равен  , а по отрезку, отсекаемому на оси ординат, определяется величина
, а по отрезку, отсекаемому на оси ординат, определяется величина 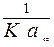 . Получаем следующие результаты:
. Получаем следующие результаты:  ; b = 0,033.
; b = 0,033.
Более точные значения параметров  и K получаются при статистической обработке данных, например, методом наименьших квадратов. Вычисляем удельную поверхность:
и K получаются при статистической обработке данных, например, методом наименьших квадратов. Вычисляем удельную поверхность:
S уд = a ¥ S 0 N A = 2,74 моль/кг . 1,86 . 10 – 19 м 2 . 6,022 . 10 23 моль – 1 = 30,7 . 10 4 м 2 /кг.
Задачи
202. При изучении адсорбции уксусной кислоты на угле при 25 0С были получены следующие данные:
| С, ммоль/ см 3 | 0,018 | 0,031 | 0,062 | 0,126 |
| a, ммоль/г | 0,467 | 0,624 | 0,801 | 1,11 |
Определить графически константы в уравнении изотермы адсорбции Фрейндлиха.
203. При изучении адсорбции уксусной кислоты на угле при 25 0С были получены следующие данные:
| С, ммоль/ см 3 | 0,268 | 0,471 | 0,882 |
| a, ммоль/г | 1,55 | 2,04 | 2,48 |
Определить графически константы в уравнении изотермы адсорбции Фрейндлиха.
204. По уравнению Фрейндлиха вычислить равновесную концентрацию уксусной кислоты, если 1 г угля адсорбирует 3,76 ммоль СН3СООН. Константа k = 2,82; n =2,44.
205. При изучении адсорбции ацетона древесным активированным углем при 20 0С были получены следующие данные:
| С, ммоль/л | 2,34 | 14,65 | 88,62 | 177,69 | 268,97 |
| a, ммоль/г | 0,208 | 0,618 | 1,50 | 2,08 | 2,88 |
Определить графически постоянные уравнения изотермы Фрейндлиха и рассчитать количество ацетона, адсорбируемое 1 г угля при равновесной концентрации ацетона 125 ммоль/л.
206. Определить постоянные уравнения Фрейндлиха, используя следующие данные для адсорбции при 231 К углекислого газа на угле:
| р (CO 2) . 10 – 3, Па | 1,00 | 4,48 | 10,00 | 14,40 | 25,00 | 45,20 |
| Адсорбция a . 10 2, кг/кг | 3,23 | 6,67 | 9,62 | 11,72 | 14,50 | 17,70 |
207. По приведенным данным об адсорбции СО2 на угле марки С при (- 42 0 С) определить константы в уравнении Фрейндлиха.
| р (СО2), Торр | 10,0 | 50,0 | ||||
| a, моль/кг | 0,659 | 1,341 | 1,545 | 2,000 | 2,341 | 2,591 |
208. По приведенным результатам адсорбции амилового спирта на активном угле марки СКТ при 20 0С составить уравнение изотермы адсорбции Ленгмюра и определить удельную поверхность угля. Площадь поперечного сечения молекул амилового спирта принять равной
1,6 . 10 – 19 м 2.
| С, моль/ м 3 | 0,94 | 1,83 | 3,10 | 5,60 | 11,05 |
| a, моль/ кг | 0,61 | 1,21 | 1,76 | 2,65 | 3,96 |
209. По приведенным данным для адсорбции уксусной кислоты на древесном угле при 25 0С составить уравнение изотермы адсорбции Фрейндлиха.
| С, моль / л | 0,05 | 0,10 | 0,50 | 1,00 | 1,50 |
| a, г / г | 0,04 | 0,06 | 0,12 | 0,16 | 0,19 |
210. По приведенным результатам адсорбции СО2 на угле марки С при (- 42 0 С) составить уравнение изотермы адсорбции Фрейндлиха.
| р (СО 2), кПа | 1,00 | 4,48 | 10,0 | 14,4 | 25,0 | 45,2 |
| a . 10 3, моль/ кг | 7,34 | 15,2 | 21,9 | 26,6 | 32,9 | 40,2 |
Задачи № 211 - 214. По приведенным данным: а) построить изотерму адсорбции; б) проверить применимость уравнения Ленгмюра; в) если изотерма не соответствует уравнению Ленгмюра, составить уравнение адсорбции Фрейндлиха.
211. Адсорбция H2S на цеолите CaX при 25 0С:
| p (H2S), Торр | |||||||||
| a, моль/кг | 0,735 | 0,882 | 1,412 | 1,559 | 1,941 | 2,118 | 2,294 | 2,471 | 2,588 |
212. Адсорбция H2S на цеолите NaA при 25 0С:
| p (H2S), Торр | |||||||||
| a, моль/кг | 2,294 | 2,941 | 3,235 | 3,529 | 3,765 | 3,882 | 4,059 | 4,176 | 4,298 |
213. Адсорбция H2S на цеолите CaА при 25 0С:
| p(H2S), Торр | |||||||||
| a, моль/кг | 1,588 | 2,824 | 3,294 | 3,765 | 4,176 | 4,353 | 4,471 | 4,647 | 4,706 |
214. Адсорбция H2S на цеолите NaХ при 25 0С:
| p (H2S), Торр | |||||||||
| a, моль/кг | 2,824 | 3,824 | 4,118 | 4,471 | 4,706 | 4,882 | 5,000 | 5,059 | 5,235 |
Задачи №№ 215 - 221. Вычислить адсорбцию (a) моль/м2 данного вещества по приведенным данным поверхностного натяжения водного раствора и воды (s):
| № | Вещество | s раствора, мДж / м 2 | Концентра ция, моль/л | s (Н2О), мДж / м 2 | Темпера тура, К |
| CH3-CH2-COOH Пропионовая кислота | 55,6 | 0,5 | 71,96 | ||
| CH3-(CH2)3-COOH Валерьяновая кислота | 52,1 | 0,5 | 75,62 | ||
| CH3COOH Уксусная кислота | 71,2 | 0,05 | 72,75 | ||
| CH3-CH2-COOH Пропионовая кислота | 67,7 | 0,05 | 72,75 | ||
| NaCl | 78,4 | 1,3 | 73,6 | ||
| NaCl | 76,9 | 2,34 | 73,6 | ||
| CH3COOH Уксусная кислота | 70,9 | 0,125 | 73,6 |
Задачи № 222 - 226. При адсорбции указанных газов на активированном угле получены следующие результаты (см. табл.). Вычислить постоянные в уравнении Лэнгмюра для газовой адсорбции.
| № | газ | Давление, Па | Количество адсорбированного газа | Т, К |
| Ar | 31,9 . 103; 130,5 . 103; 290 . 103 | 5; 15,4; 24 мг/г | 194,7 | |
| Kr | 1,35 . 104; 2,63 . 104; 3,93 . 104 | 0,15; 0,27; 0,38 моль/г | ||
| CO | 6,63 . 104; 7,94 . 104; 9,25 . 104 | 0,55; 0,62; 0,68 моль/г | ||
| CO2 | 4,8 . 10-1; 11,9 . 10-1; 20,6 . 10-1 | 0,122; 0,195; 0,255 моль/г | ||
| N2 | 2,8 . 10-1; 6,1 . 10-1; 17,3 . 10-1; | 0,65; 0,75; 0,85 моль/г |
Задачи № 227 - 229. Построить изотерму поверхностного натяжения, используя значения поверхностных натяжений водных растворов данных веществ при указанной температуре (см.табл.), если поверхностное натяжение воды при 293 К равно 72,75 м Дж / м2, а при 298 К – 71,96 м Дж/м 2. Определить графически адсорбцию вещества при указанной концентрации.
| № | вещество | С (ПАВ), ммоль/л | s ж - г , м Дж/м2 | С х, ммоль/л | Т, К |
| Додецилсульфат натрия | 2,16; 3,96; 6,6; 8,3; 9,3; 9,8; 10,2; 11,2 | 62; 54; 47; 43; 42; 41; 41; 41 | 5,0 | ||
| Уксусноэтиловый эфир | 7,8; 15,6; 31,2; 62,5; 12,5; 250; 500 | 69,6; 68; 65,8; 61,5; 56,2; 49,7; 41,5 | 20,0 | ||
| Уксусноэтиловый эфир | 5,3; 7,4; 19,5; 30,2; 60,7; 120,8; | 63; 62,2; 60,1; 54,2; 48,5; 40,3 | 50,0 |
№ 230. По приведенным результатам массовой адсорбции пентанола на активированном угле при температуре 20°С построить изотерму адсорбции и составить уравнение адсорбции.
| С, моль/м 3 | 0,94 | 1,83 | 3,1 | 5,6 | 11,05 |
| a, моль/ кг | 0,61 | 1,21 | 1,76 | 2,65 | 3,96 |
№ 231 - 236. Определить поверхностную активность вещества по указанным данным.
| № | Вещество | s , мДж/м2 | s (Н2О), мДж/м 2 | Т, (К) | С.ПАВ, моль/л |
| CH3-CО-O-C2H5 уксусноэтиловый эфир | 71,96 | 15,6 | |||
| CH3COOH уксусная кислота | 71,2 | 72,75 | 0,05 | ||
| CH3-CH2-COOH пропионовая кислота | 67,7 | 72,75 | 0,05 | ||
| CH3-CH2-COOH пропионовая кислота | 55,6 | 71,96 | 0,5 | ||
| CH3-(CH2)3-COOH валерьяновая кислота | 52,1 | 75,62 | 0,5 | ||
| CH3COOH уксусная кислота | 71, 2 | 72,75 | 0,125 |
237 - 240. Определить площадь занимаемую молекулой вещества (указанного в табл.) в насыщенном адсорбционном слое активированного угля.
| № | Название вещества | a Ґ - предельная адсорбция |
| C3H7OH пропанол | 5,3 . 10 - 10 (моль/см2) | |
| CH3-CH-COOH изомасляная кислота | CH3 | 5,4 . 10 - 9 (кмоль/м2) | |
| C6H5NH2 анилин | 6,01 . 10 - 9 (кмоль/м2) | |
| C5H11OH пентанол | 5,3 . 10 – 10 (моль/см2) |
ЛИТЕРАТУРА
1. Краткий справочник физико-химических величин / Под. ред. А. А. Равделя и А.М. Пономаревой. Л.: Химия, 1983.
2. Д. Сталл, Э. Вестрам, Г. Зинке. Химическая термодинамика органических соединений. М.: Мир, 1971.
3. Физическая химия т.1, т. 2 / К.С. Краснов, Н.К. Воробьев, И. Н. Годнев и др. М.: Высшая школа, 1995.
4. И.В. Кудряшов, Г.С. Каретников «Сборник примеров и задач по физической химии»,1991, Москва, «Высшая школа».
5. Задачи по физической химии / В. В. Еремин, С. И. Каргов, И. А. Успенская и др. – М.: Изд-во «Экзамен», 2003. – 320 с.
6. Бадаев Ф. З., Батюк В. А. Цепные реакции. Москва, Изд-во МТГУ, 1995.
7. Химическая термодинамика. Методические указания. / Е. Е. Гончаренко, В. А. Батюк, Н. М. Елисеева и др. М.: Изд-во МГТУ, 1994.
Содержание
1. Зависимость термодинамических функций от температуры
Последнее изменение этой страницы: 2016-08-11
lectmania.ru. Все права принадлежат авторам данных материалов. В случае нарушения авторского права напишите нам сюда...