
Категории:
ДомЗдоровьеЗоологияИнформатикаИскусствоИскусствоКомпьютерыКулинарияМаркетингМатематикаМедицинаМенеджментОбразованиеПедагогикаПитомцыПрограммированиеПроизводствоПромышленностьПсихологияРазноеРелигияСоциологияСпортСтатистикаТранспортФизикаФилософияФинансыХимияХоббиЭкологияЭкономикаЭлектроника
Смещение химического равновесия
При изменении условий протекания реакции (температуры, давления, концентрации какого-либо из участвующих в реакции веществ) скорости прямого и обратного процессов изменяются неодинаково, и химическое равновесие нарушается.
Направление смещения химического равновесия подчиняется принципу Ле-Шателье:
если на систему, находящуюся в состоянии химического равновесия, оказать какое-либо воздействие, то равновесие сместится в таком напрвлении, что оказанное воздействие будет ослаблено.
При увеличении температуры равновесие смещается в сторону реакции идущей с поглощением тепла - эндотермической.
При увеличении концентрации исходных веществ равновесие смещается в сторону образования продуктов реакции, т.е. вправо.
При увеличении концентрации продуктов реакции равновесие смещается в сторону образования исходных веществ , т.е. влево.
Если реакция протекает с участием газообразных веществ, то повышение давления вызывает смещение равновесия в направлении уменьшения общего числа молей. Понижение давления смещает равновесие в сторону увеличения общего числа молей газообразных веществ.
Например, равновесие системы:
N2 + 3H2 Û 2NH3;
DH = -46,25 кДж/моль
а) при увеличении температуры сместится влево;
б) при увеличении давления сместится вправо;
в) при увеличении концентрации азота сместится вправо.
Экспериментальная часть
Опыт 1. Влияние концентрации реагирующих веществ
На состояние химического равновесия
В результате обратимой реакции
FeCl3 + 3KSCN Û Fe(SCN)3 + 3KCl
образуется интенсивно окрашенное в красный цвет вещество роданид железа(III) Fe(SCN)3. Поскольку интенсивность окраски раствора зависит от концентрации окрашенного вещества, то судить о смещении равно-весия в данной системе можно по изменению интенсивности окраски раствора.
а) Налить почти полную пробирку дистиллированной воды и добавить в нее по 1-2 капли концентрированных растворов хлорида железа(III) FeCl3 и роданида калия KSCN. Раствор перемешать и затем разлить содержимое в четыре пробирки. Первую пробирку оставить для сравнения, во вторую прибавить 2-3 капли хлорида железа (III) FeCl3, в третью 2-3 капли роданида калия KSCN, а в четвертую - несколько кристалликов хлорида калия KСl. Пробирки встряхнуть несколько раз. Сравнить интенсивность окрасок раствора во 2-й, 3-й и 4-й пробирках с окраской первой (контрольной) пробирки. Определить, в какой пробирке и в каком направлении прошло смещение химического равновесия. Как изменится в каждом отдельном случае концентрация компонентов равновесной системы:
1) роданида железа Fe(SCN)3
2) хлорида железа (III) FeCl3
3) роданида калия КSCN, по сравнению с их концентрациями при установлении первоначального равновесия?
Результаты наблюдения занести в таблицу 6.1.
Таблица 6.1
Результаты опыта №1
| № пробирок | Содержание пробирок | Цвет раствора | Направление смещения равновесия | Заключение об изменении концентрации компонентов | |||
| FeCl3 | KSCN | Fe(SCN)3 | KCl | ||||
| конр.р-р | |||||||
| к.р.+FeCl3 | |||||||
| к.р.+КSCN | |||||||
| к.р.+KCl |
Написать выражение константы равновесия. Объяснить влияние концентрации реагирующих веществ на смещение химического равновесия.
б) Налить половину пробирки дистиллированной воды, добавить 2-3 капли гидроксида аммония NH4OH и 2 капли фенолфталеина. Раствор перемешать. Отметить цвет раствора. Наличие, каких ионов придает раствору окрашивание?
Написать выражение константы диссоциации слабого электролита NH4OH.
Разлить содержимое на две части. Первую пробирку оставить в качестве эталона, а к содержимому второй пробирки добавить несколько кристалликов хлорида аммония NH4Cl. Отметить изменение цвета раствора. Написать уравнение диссоциации NH4Cl. За счет каких ионов происходит смещение равновесия в данной системе, в каком направлении?
Опыт 2. Влияние температуры на состояние
химического равновесия
При взаимодействии йода с крахмалом образуется йод-крахмальное соединение сложного состава, имеющее синюю окраску. Реакция сопровождается выделением тепла. Равновесие данной системы можно условно представить схемой:
йод + крахмал Û [йод – крахмал], DН0<0
В пробирку налейте 10 капель дистиллированной воды, 2-3 капли раствора йода и добавьте 2-3 капли крахмала. Отметьте появление синей окраски. Пробирку нагрейте до кипения. Наблюдайте изменение окраски раствора. Затем пробирку охладите водой из-под крана. Наблюдайте вновь появление синей окраски.
В каком направлении смещается равновесие этой системы при нагревании и при охлаждении?
Лабораторная работа №3(2)
Скорость химических реакций
Химические реакции протекают с различными скоростями. Скорость и механизм химических превращений изучает особый раздел химии - химическая кинетика. Знание законов химической кинетики имеет большое научное и практическое значение.
Химические реакции могут протекать в однородных системах, состоящих из одной фазы, и неоднородных, состоящих из нескольких фаз.
Системой в химии принято называть вещество или совокупность веществ, физически ограниченных от внешней среды.
Фаза - однородная часть системы, обладающая на всем протяжении одинаковыми свойствами и отделенная от других частей системы поверхностью раздела.
Система, состоящая из одной фазы, называется гомогенной (газовая смесь - воздух, смесь воды и спирта).
Реакция, протекающая в такой системе, называется гомогенной.
Система, состоящая из нескольких фаз, называется гетерогенной (вода со льдом).
Реакция, протекающая в такой системе, называется гетерогенной.
В гомогенной системе реакция идет во всем объеме этой системы. Например, при сливании растворов серной кислоты и гидроксида натрия реакция идет во всем объеме раствора:
H2SO4 + 2NaOH = Na2SO4 + 2H2O.
В гетерогенных системах реакция протекает только на поверхности раздела фаз, образующих систему. Например, растворение металла в кислоте протекает на поверхности металла, потому что только здесь соприкасаются друг с другом реагирующие вещества:
Zn + 2НСl = ZnCl2 + Н2  .
.
В связи с этим скорость гомогенной и гетерогенной реакции определяются различно.
Скорость гетерогенной реакции определяется количеством вещества, вступающего в реакцию или образующегося при реакции за единицу времени на единице поверхности раздела фаз.
Скорость гомогенной реакции определяется количеством вещества, вступающего в реакцию или образующегося при реакции за единицу времени в единице объема системы.
Если реакции в гомогенной системе протекают при постоянном объеме, то ее скорость может быть определена через изменение концентрации реагирующих веществ за единицу времени.
Для вещества, вступающего в реакцию, это определение может быть выражено уравнением:
n = -DC / Dt , моль/л * сек
а для образующегося вещества
n = DC / Dt , моль/л * сек
где DC - изменение концентрации вещества за время Dt, моль/л.
Знаки в правой части этих уравнений различны, так как в ходе реакции концентрации исходных веществ убывают (DC < 0), а для образующихся продуктов – возрастают (DC > 0).
Скорость реакции зависит от природы реагирующих веществ, их концентрации, температуры и от присутствия в системе катализатора.
В тех случаях, когда при протекании реакции необходимо столкновение двух реагирующих частиц (молекул, атомов), зависимость скорости реакции от концентрации определяется законом действия масс:
при постоянной температуре скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ в степени их стехиометрических коэффициентов.
Например, если реакция протекает по уравнению:
2NOгаз + O2 газ = 2NO2 газ .
то выражение закона действия масс запишется следующим образом:
V= К [NO]2 * [О2],
где V- скорость реакции,
К- константа скорости.
Величина константы скорости К зависит от природы реагирующих веществ, от температуры и от присутствия катализатора, но не зависит от концентрации веществ.
В случае гетерогенных реакций в уравнении закона действия масс входит концентрация только тех веществ, которые находятся в газовой фазе или в растворе. Концентрация вещества, находящегося в твердой фазе, обычно представляет собой постоянную величину и поэтому входит в константу скорости.
Например, для реакции горения угля
C тв + O2 газ = CO2 газ,
закон действия масс пишется так:
V = К * [O2].
Зависимость скорости химической реакции от температуры подчиняется эмпирическому закону Вант-Гоффа:
при повышении температуры на каждые 10°С скорость химических реакции, увеличивается примерно в 2-4 раза
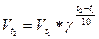 ,
,
где g - температурный коэффициент скорости реакции, значение которого лежит в пределах 2-4; 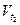 - скорость реакции при температуре t2 0C;
- скорость реакции при температуре t2 0C; 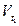 - cкорость реакции при температуре t1 0C.
- cкорость реакции при температуре t1 0C.
Экспериментальная часть
Последнее изменение этой страницы: 2016-08-11
lectmania.ru. Все права принадлежат авторам данных материалов. В случае нарушения авторского права напишите нам сюда...