
Категории:
ДомЗдоровьеЗоологияИнформатикаИскусствоИскусствоКомпьютерыКулинарияМаркетингМатематикаМедицинаМенеджментОбразованиеПедагогикаПитомцыПрограммированиеПроизводствоПромышленностьПсихологияРазноеРелигияСоциологияСпортСтатистикаТранспортФизикаФилософияФинансыХимияХоббиЭкологияЭкономикаЭлектроника
Нормирование химического фактора.
Санитарно-гигиенические нормативы.
Вредный производственный фактор – производственный фактор, воздействие которого на работающего, в определённых условиях, приводит к заболеванию или снижению работоспособности.
Опасный производственный фактор – производственный фактор, воздействие которого на работающего, в определённых условиях, приводит к травме или другому внезапному ухудшению здоровья.
Вредный производственный фактор, в зависимости от интенсивности и продолжительности воздействия, может стать опасным.
ПДК (предельно-допустимая концентрация) – установленный безопасный уровень вещества в воздухе рабочей зоне (возможно в почве, воде, снеге) соблюдение которого позволяет сохранить здоровье работника в течение рабочей смены, нормального производственного стажа и по выходу на пенсию. Не передаётся негативное последствие на последующие поколения.
ПДУ (предельно-допустимый уровень) – характеристика, применяемая к физическим опасным и вредным производственным факторам (по ГОСТ 12.0.002-80) - это предельное значение величины вредного производственного фактора, воздействие которого при ежедневной регламентированной продолжительности в течение всего трудового стажа не приводит к снижению работоспособности и заболеванию как в период трудовой деятельности, так и к заболеванию в последующий период жизни
Вредные условия труда – это условия труда, характеризующиеся наличием вредных производственных факторов, превышающих гигиенические нормативы и оказывающие неблагоприятное воздействие на организм работающего и (или) его потомство.
ОБУВ - Ориентировочный безопасный уровень воздействия загрязняющего атмосферу вещества, временный гигиенический норматив для загрязняющего атмосферу вещества, устанавливаемый расчетным методом для целей проектирования промышленных объектов (ГОСТ 17.2.1.03-84).
Сильнодействующие ядовитые вещества́ (СДЯВ) — химические соединения, обладающие высокой токсичностью и способные при определенных условиях (в основном при авариях на химически опасных объектах) вызывать массовые отравления людей и животных, а также заражать окружающую среду. В настоящее время взамен термина СДЯВ используется термин Аварийно химически опасное вещество́ (АХОВ).
Основные особенности СДЯВ:
способность по направлению ветра переноситься на большие расстояния, где и вызывать поражение людей;
объемность действия, то есть способность зараженного воздуха проникать в негерметизированные помещения;
большое разнообразие СДЯВ, что создает трудности в создании фильтрующих противогазов;
способность многих СДЯВ оказывать не только непосредственное действие, но и заражать людей посредством воды, продуктов, окружающих предметов.
Аварийно химически опасное вещество (АХОВ) - опасное химическое вещество, применяемое в промышленности и сельском хозяйстве, при аварийном выбросе (разливе) которого может произойти заражение окружающей среды в поражающих живой организм концентрациях (токсодозах).
Токсодоза - значение заражения, равное произведению концентрации ОХВ на время пребывания человека в данном месте без средств защиты органов дыхания, в течение которого проявляются различные степени токсического воздействия ОХВ на человека (первые слабые признаки отравления - пороговая токсодоза; существенное отравление - поражающая токсодоза; кома - смертельная токсодоза). Основные виды токсических доз: ингаляционная, кожно-резорбтивная и внутримышечная (при ранении заражёнными осколками). В качестве ингаляционной Т.д. используется величина Ct (C - концентрация ОВ в воздухе, мг/л; t - экспозиция, мин); для др. видов Т.д. - D (масса ОВ, приходящегося на килограмм массы человека, мг/кг). По степени поражения Т.д. подразделяется на категории: летальную (LCt50, LD50), выводящую из строя (ICt50, ID50), лёгкую (ECt50, ED50) и пороговую (PCt50, PD50). Эффект поражения, соответствующий любой категории Т.д., достигается в 50 % случаев (это отражается индексом). Часто Т.д. LCt50 (LD50) называется среднелетальной, а ICt50 (ID50) - средневыводящей из строя.
Обоняние.
Обоняние (olfactus) - вид чувствительности, направленной на восприятие запахов; осуществляется обонятельным анализатором. Периферическая часть обонятельного анализатора представлена рецепторными клетками (обонятельным эпителием), расположенными в слизистой оболочке верхнезадней части полости носа (Придаточные пазухи носа), в области верхней носовой раковины и прилежащей к ней части носовой перегородки (у человека их насчитывается около 10 млн., у собаки-овчарки — свыше 200 млн.), и обонятельным нервом, образованным аксонами рецепторных клеток..
У человека обоняние играет значительно меньшую роль, чем у животных и чем другие виды сенсорного восприятия — зрение и слух. Его роль возрастает при слепоте и особенно слепоглухоте; при этом наблюдается компенсаторное развитие обонятельной чувствительности, выраженной способности к анализу запахов, обонятельной памяти.
Рецепцию пахучих веществ осуществляют рецепторные клетки. Их периферические отростки снабжены булавовидными утолщениями, заканчивающимися пучком тонких обонятельных волосков (жгутиков, или ресничек), погруженными в слой слизи. Обонятельные волоски увеличивают общую поверхность обонятельных клеток в десятки раз.
. Сигналы от рецепторных клеток по нервным волокнам поступают в головной мозг, где происходит формирование впечатления о характере запаха (качестве, силе), его узнавание и др. Многие вещества, обладающие резким запахом (например, аммиак, муравьиная и уксусная кислоты), наряду с обонятельным оказывают действие, раздражающее чувствительные волокна тройничного нерва, что обусловливает специфику формирования ощущения запаха. Обонятельные раздражители рефлекторно могут также изменять частоту дыхательных движений и пульса, кровяное давление. Представляет интерес феномен так называемого гематогенного обоняния (появление ощущения запаха после введения в кровь раствора пахучего вещества), механизм которого еще недостаточно изучен.
Для многих пахучих веществ определен порог восприятия (так называемый порог обоняния), т.е. минимальная концентрация вещества, способная вызвать реакцию обонятельного анализатора (порог узнавания, когда воспринимается качество запаха, обычно лежит несколько выше порога обоняния) [2], [4], [5], [6], [7], [8], [9].
Выполнил Соловьев А.
Спектрофотометрия.
Спектрофотометрией называется метод количественного анализа, основанный на определении концентрации вещества по спектру поглощения. Анализ проводят следующим образом. Через анализируемый раствор (иногда газ, или даже твердое тело) пропускают пучок видимого или невидимого света известной длины волны (ультрафиолетовой (200—400 нм), видимой (400—760 нм) и инфракрасной (>760 нм)). По тому, какая часть этого света поглощается раствором, заключают о концентрации поглощающего свет вещества[10].
Законы поглощения света.
Закон Ламберта. Относительное количество поглощенного пропускающей средой света не зависит от интенсивности падающего излучения; все последующие слои среды поглощают равные доли проходящего через них света. Математически этот закон выражается так:

I0 – интенсивность падающего света;
I – интенсивность пропущенного света;
l – толщина поглощающего слоя (см);
К – постоянная (коэффициент погашения по Бунзену и Роско). Очевидно, что в постоянную К не входит концентрация поглощающего вещества. Влияние концентрации учитывается другим важным законом - законом Бера: поглощение света пропорционально числу молекул вещества, через которое проходит свет. Таким образом, если поглощающее вещество растворено в полностью прозрачном растворителе, поглощение раствора будет пропорционально его молярной концентрации.
Подстановка величины εС (ε – молярный коэффициент экстинкции (погашения) (л*моль/см) и С – концентрация, выраженная в грамм-молях на литр) вместо К в приведенном выше уравнении для закона Ламберта приводит к соотношению

На этом выражении, объединяющем законы Ламберта и Бера, основывается большинство применений спектрофотометрии в химических исследованиях. Для удобства величину lg(I0/I) обозначают символом А (абсорбционное отношение). В отечественной литературе приняты термины «экстинкция» (погашение) (Е) или «оптическая плотность» (D).
Из закона Бера следует, что если при изменении концентрации раствора и толщины поглощающего слоя произведение этих величин остается постоянным, интенсивность поглощения раствора также должна быть постоянной.
При применении абсорбционной спектрофотометрии считается обязательным проверять справедливость закона Бера для каждого вещества. Для большей части неионизированных органических соединений закон Бера выполняется по крайней мере приближенно. Если раствор или растворитель очень сильно поглощают, немонохроматическое излучение может составить значительную долю от общего светового потока, попадающего на детектор. Такие трудности особенно существенны в дальней УФ области спектра, вблизи полос поглощения атмосферного кислорода; поэтому необходимо либо вакуумировать спектрометр, либо продувать его прозрачным в этой области газом, например азотом [12].
Если концентрация выражена в граммах на 1 л, то соответствующее значение ε называют удельным коэффициентом погашения. Если в г-молях , то молярным коэффициентом погашения. ε зависит от природы поглощающего вещества, длины волны света, от температуры и не зависит от растворителя. Коэффициент экстинкции для конкретного вещества – это величина характеризующая эффективность поглощения света; чем труднее свет проходит через раствор, тем выше коэффициент экстинкции [11].
Приборы и методы измерений.
Фотографические методы. Спеккер-фотометр. В этом приборе источник света, обычно искра между электродами из вольфрамовой стали или водородная лампа, установлен непосредстенно на фотометре. Пучок света расщепляется на два луча одинаковой интенсивности, которые затем проходят через оптически идентичные кюветы, одна из которых содержит исследуемый раствор, а другая чистый растворитель. Количество света, прошедшего через кювету сравнения, регулируется при помощи микрометрического винта, уменьшающего площадь одного из отверстий, через которое свет попадает на фотометр. Микрометрический винт связан с указателем, перемещающимся вдоль спиральной прорези в барабане, отградуированном непосредственно в значениях оптической плотности от 0,1 до 2,0. При этом отношение I0/I представляет также отношение площадей отверстий в пучке сравнения и в пучке, проходящем через раствор, соответственно. Получающиеся спектры фотографируют друг под другом и затем, рассматривая пары спектров, для точек равного почернения строят графики зависимости оптической плотности от длины волны. Спектрографические методы измерения спектров поглощения дают возможность сразу оценить весь фотографируемый спектральный интервал и в этом отношении имеют некоторое преимущество перед фотоэлектрическими методами. Это особенно важно при спектральных исследованиях неустойчивых промежуточных продуктов.

Рис.1. Оптическая схема спеккер-фотометра.
1-источник света; 2- кварцевые ромбы; 3 – линзы; 4- отверстия фотометра; 5- барабан для установки меньшей аппаратуры (пучок сравнения); 6 – абсорбционные кюветы; 7 – линзы; 8- кварцевые ромбы.
[12].
Фотоэлектрические методы. Недостатки этого метода: они требуют большой затраты времени и применения дорогих фотоматериалов; кроме того, регистрация интенсивностей на фотопластинке дает невысокую точность результатов, не превышающую, по-видимому, ±2%, а суммарная ошибка фотографических методов может быть >4%. Однако современные фотоэлектрические приборы значительно более удобны в обращении, являются быстродействующими и позволяют измерять оптическую плотность с точностью до ±0,2%. Благодаря этому фотоэлектрические методы стали широко применяться в спектрофотометрии. В отличие от фотографических спектрофотометров с регистрацией на фотопластинке современные фотоэлектрические приборы имеют один или несколько фотоэлементов или фотоумножителей с чувствительностью обеспечивающей регистрацию всего исследуемого спектрального интервала. Фотоэлектрические спектрофотометры особенно удобны для количественных измерений интенсивности при данной длине волны.

Рис.2. Оптическая схема спектрофотометров (СФ-4, СФД-2, СФ-5):
1- источник излучения; 2-зеркало конденсатор; 3-плоское зеркало; 4-щель монохроматора; 5-зеркальный объектив; 6-кварцевая диспергирующая призма или дифракционная решетка; 7-кювета; 8-линза; 9-фотоэлемент.
Световой пучок от источника света попадает в монохроматор через входную щель и разлагается дифракционной решеткой или призмой в спектр. В монохроматический поток излучения, поступающий из выходной щели в кюветное отделение, поочередно вводятся контрольный и исследуемый образцы. Излучение, прошедшее через кювету, попадает на фотоэлемент, который преобразовывает световую энергию в электрическую. Электрический сигнал затем усиливается и регистрируется.
Монохроматоры. Монохроматор – это оптическая система, выделяющая из всего спектра источника света излучение определенной длины волны. Это обычно призмы, по-разному преломляющие свет разных длин волн, или дифракционные решетки. В видимой области используются обычные стеклянные призмы, но в ультрафиолетовой области они не годятся, поскольку стекло начинает поглощать уже при λ < 400 нм, поэтому призмы делают из кварца.
В качестве монохроматоров применяются также дифракционные решетки, которые представляют собой плоскопараллельную пластину с нанесенными на ней параллельными линиями – бороздками. Белый свет из-за дифракции на параллельных бороздках разлагается на непрерывный спектр. Обычно в монохроматорах сначала выделяют пучок света с определенным диапазоном длин волн с помощью призмы, а затем разлагают его еще раз решеткой. Так получают строго монохроматический свет. Основное достоинство дифракционных решеток состоит в том, что можно увеличивать их разрешающую способность, поскольку она прямо пропорциональна плотности линий. Кроме того, во всем диапазоне длин волн дифракционные решетки имеют линейное разрешение, тогда как разрешение призменного монохроматора с увеличением длины волны уменьшается.
Кюветы. Исследуемое вещество растворяют в соответствующем растворе и помещают в оптически прозрачный сосуд для измерений – кювету. Поскольку стекло поглощает ультрафиолетовый свет, для проведения измерений в ультрафиолетовой области спектра используют кварцевые кюветы. Для измерений в видимой области можно использовать пластиковые или стеклянные кюветы. При работе с летучими или химически активными веществами кюветы закрывают крышками.
Поскольку кювета, помещенная в спектрофотометр, становится составной частью его оптической системы, с ней нужно обращаться очень аккуратно. Царапины и грязь на стенках кюветы сильно рассеивают и поглощают свет, искажая результаты измерений. Об этом особенно надо помнить при работе в ультрафиолетовой области. Кюветы можно протирать мягкими тканями, например, из хлопка. Не рекомендуется использовать для этих целей фильтровальную бумагу. Поскольку органические молекулы поглощают в ультрафиолетовой области, ни в коем случае нельзя касаться оптических (прозрачных) стенок кюветы. Раствор лучше заливать в кювету, поставив ее в предварительно вынутый из прибора кюветодержатель. Кюветы довольно хрупки, особенно кварцевые, поэтому работать с ними надо осторожно, не допуская механических повреждений.
Содержимое кюветы должно быть гомогенным – это необходимое условие получения воспроизводимых данных. Нужно следить за тем, чтобы раствор не был мутным. Особенно мешают измерениям пузырьки воздуха, сильно увеличивающие рассеяние. Нельзя наливать в кювету очень холодный раствор, поскольку при этом на наружных стенках кюветы конденсируются пары воды воздуха, и стенки становятся непрозрачными.
Если кюветы загрязнены посторонними примесями, их следует промыть дистиллированной водой и (или) растворителем, в котором растворено исследуемое вещество. Кюветы можно мыть мягкими детергентами. Не рекомендуется мыть кюветы концентрированными кислотами или щелочами, а также другими травящими агентами.
Кюветы нужно заполнять до такого уровня, чтобы поток излучения проходил целиком через слой раствора. Чаще всего используются кюветы с оптическим путем 1 см, в которые обычно заливают 2,5–3 мл раствора. В такие кюветы входит 4–5 мл, но заполняют их полностью лишь в том случае, когда это необходимо. Есть кюветы с оптическим путем 0,01; 0,05; 0,1; 0,2; 0,5; 1,0; 2,0; 4,0; 10,0 см.
Фотоэлементы. Фотоэлементы преобразовывают световую энергию в электрическую. Электрический сигнал затем усиливается и регистрируется.
Фотоны, бомбардируя поверхность фотоэлемента, выбивают из него электроны, количество которых пропорционально интенсивности света. Эти электроны летят к положительному электроду. В результате в замкнутой цепи возникает электрический ток, который регистрируется по падению напряжения на сопротивлении, находящемся в этой цепи. Напряжение можно усилить, и после компенсации такого сигнала потенциометром, отградуированном в единицах поглощения, на датчике регистрируется непосредственно поглощение образца.
Фотоумножители обычно более чувствительны, чем простые фотоэлементы. Это происходит из-за того, что электроны, вылетевшие из фоточувствительного слоя, ускоряются высоким напряжением, а из-за соударений в газе возникают вторичные электроны, что и приводит к возрастанию тока
Ширина щели. От размера щели зависит диапазон длин волн света, падающего на образец. Поэтому для получения надежных результатов надо работать при минимально узкой для данных условий эксперимента щели. Если щель выбрана правильно, то при изменении ее размеров вдвое показания прибора не меняются.
Обычно нулевое значение поглощения устанавливают щелью, но в хороших спектрофотометрах это делают, изменяя напряжение фотоэлемента. Такая регулировка позволяет работать при постоянной ширине щели. [11]
Принципиальная схема спектрофотометра представлена на рисунке 3. Свет разлагается на составляющие его длины волн с помощью одинарного монохроматора. Затем в фотометре расщепляется на два луча, один из которых проходит через кювету сравнения, а другой – кювету, содержащую раствор излучаемого вещества. Затем прошедшие через обе кюветы лучи автоматически сравниваются регистрируются в виде спектра.

Рис. 3. Принципиальная схема спектрофотометра.
Отбор пробы воздуха
Отбор проб проводят с учетом требований ГОСТ 12.1.005-88 "ССБТ. Общие санитарно-гигиенические требования к воздуху рабочей зоны" и Руководства Р 2.2.2006-05 (прилож. 9, обязательное) "Общие методические требования к организации и проведению контроля содержания вредных веществ в воздухе рабочей зоны", пункт 2 "Контроль соответствия максимальным ПДК".
Воздух с объемным расходом 2 куб. дм/мин. аспирируют через последовательно соединенные фильтр АФА-ХА-20, помещенный в фильтродержатель, и поглотительный прибор Яворовской, заполненный 2 г силикагеля.
Для измерения 1/2 ОБУВ пиретрума необходимо отобрать 10 куб. дм воздуха. Отобранные пробы могут храниться в бюксах в течение недели.
Выполнение измерений
После отбора пробы фильтр с помощью пинцета переносят в бюкс и заливают 5,0 куб. см гексана. Оставляют на 10 - 15 минут, периодически помешивая стеклянной палочкой для лучшего растворения вещества. Затем фильтр отжимают, раствор сливают в пробирку, объем доводят до 5,0 куб. см гексаном, а фильтр повторно заливают 5,0 куб. см гексана, оставляют на 10 - 15 минут, периодически помешивая стеклянной палочкой для лучшего растворения вещества. Затем фильтр отжимают, раствор сливают в другую пробирку, объем доводят до 5,0 куб. см гексаном. Полученные растворы анализируют отдельно. Оптическую плотность полученных растворов измеряют аналогично градуировочным растворам по отношению к раствору сравнения, который готовят одновременно с анализируемой пробой, используя чистый фильтр.
Количественное определение содержания пиретрума (в мкг) в анализируемом объеме раствора пробы проводят по предварительно построенной градуировочной характеристике.
После отбора пробы силикагель из поглотительного прибора переносят в пробирку и заливают 5,0 куб. см гексана. Помещают в ультразвуковую баню на 15 минут (для лучшей десорбции вещества с силикагеля). Раствор сливают в пробирку, доводят объем до 5,0 куб. см гексаном (табл. 3) и измеряют оптическую плотность растворов в кюветах с толщиной оптического слоя 10 мм при длине волны 260 нм по отношению к раствору сравнения (раствор N 1), который готовят одновременно с градуировочными растворами, используя чистый силикагель.
3.3.4. МУК 4.1.1956-05. Методы контроля. Химические факторы. Определение концентрации нефти в почве методом инфракрасной спектрофотометрии. Методические указания [16].
Методические указания по ИК-спектрофотометрическому определению нефти в почве предназначены для использования лабораториями центров гигиены и эпидемиологии, санитарных лабораторий промышленных предприятий, лабораторий научно-исследовательских институтов, работающих в области гигиены окружающей среды. Методические указания разработаны с целью обеспечения аналитического контроля загрязнения почвы в районах расположения предприятий по добыче и переработке нефти, магистральных нефтепроводов и районов после ликвидации загрязнения в результате разлива нефти.
Измерение концентраций нефти (Н) в почве основано на экстракции нефтяных углеводородов четыреххлористым углеродом, хроматографическом отделении от полярных соединений на оксиде алюминия и количественном определении на ИК-спектрофотометре.
[10], [11], [12], [13], [14], [15], [16].
Выполнила Вербицкая Т.
Хроматография.
Хроматография – это метод разделения компонентов смеси, основанный на различии в равновесном распределении их между двумя несмешивающимися фазами, одна из которых подвижна, а другая неподвижна. Неподвижнойфазой служит твердое пористое вещество (часто его называют сорбентом). Подвижнаяфаза представляет собой жидкость или газ, протекающий через неподвижную фазу, иногда под давлением. Компоненты анализируемой смеси (сорбаты) вместе с подвижной фазой передвигаются вдоль неподвижной фазы, которую помещают в колонку. В зависимости от силы взаимодействия с поверхностью сорбента компоненты будут перемещаться вдоль колонки с разной скоростью. За счет различия в сродстве компонентов смеси к неподвижной и подвижной фазам достигается основная цель хроматографии - разделение за приемлемый промежуток времени смеси на отдельные полосы (пики) компонентов по мере их продвижения по колонке с подвижной фазой.
4.3. Классификация хроматографических методов.
Классификация возможно по агрегатному состоянию фаз, механизму разделения, по способу проведения процесса, по цели проведения процесса.
Классификация по агрегатному состоянию фаз:
-газовая (подвижная фаза - газ); газожидкостная (подвижная фаза – газ, неподвижная фаза - жидкость); жидкостная (подвижная фаза - жидкость) хроматографии.
Классификация по механизму разделения.
- Адсорбционная хроматография основана на избирательной адсорбции (поглощении) отдельных компонентов анализируемой смеси соответствующими адсорбентами. Адсорбционная хроматография подразделяется на жидкостную (жидкостно-адсорбционная хроматография) и газовую (газо-адсорбционная хроматография).
- Ионообменная хроматография основана на использовании ионообменных процессов, протекающих между подвижными ионами адсорбента и ионами электролита при пропускании раствора анализируемого вещества через колонку, заполненную ионообменным веществом (ионитом). Иониты представляют собой нерастворимые неорганические и органические высокомолекулярные соединения. В качестве ионитов применяют окись алюминия, разнообразные синтетические органические ионообменные вещества – ионообменные смолы.
- Осадочная хроматография основана на различной растворимости осадков, образуемых компонентами анализируемой смеси со специальными реактивами. Например, при пропускании раствора смеси солей Нg (II) и Pb через колонку с носителем, предварительно пропитанным раствором KI, образуются 2 окрашенных слоя: верхний, окрашенный в оранжево-красный цвет (HgI2), и нижний, окрашенный в желтый цвет (PbI2).
Классификация по способу проведения процесса.
- Колоночная хроматография - вид хроматографии, в которой в качестве носителя для неподвижного растворителя используют колонку.
- Бумажная хроматография – вид хроматографии, в которой в качестве носителя для неподвижного растворителя вместо колонки используют полоски или листы фильтровальной бумаги, не содержащей минеральных примесей.
- Тонкослойная хроматография – вид хроматографии по своему механизму разделения аналогичный бумажной хроматографии. Различие между ними заключается в том, что вместо листов бумаги разделение проводят на пластинках, покрытых тонким слоем сорбента, изготовленного из порошкообразной окиси алюминия, целлюлозы, силикагеля и т.п. и удерживающего неподвижный растворитель. Основное достоинство тонкослойной хроматографии заключается в несложности аппаратуры, простоте и большой скорости проведения эксперимента, достаточной четкости разделения смеси веществ и в возможности анализа ультрамикроколичеств вещества.
Классификация по цели проведения хроматографического процесса.
- Наибольшее значение хроматография имеет как метод качественного и количественного анализа смесей веществ (аналитическая хроматография).
- Препаративная хроматография - вид хроматографии, проводимый с целью выделения индивидуальных соединений из смеси в чистом виде. Задачей препаративной хроматографии может быть также концентрирование и последующее выделение из смеси веществ, содержащихся в виде микропримесей к основному веществу.
- Неаналитическая хроматография – вид хроматографии, который используется в качестве метода научного исследования. Ее применяют для исследования свойств систем, например растворов, кинетики химических процессов, свойств катализаторов и адсорбентов.
Газовая хроматография
Газовая хроматография – метод разделения летучих соединений, где подвижной фазой служит инертный газ (газ-носитель), протекающий через неподвижную фазу, имеющую большую поверхность. В качестве подвижной фазы можно использовать водород, гелий, азот, аргон и углекислый газ. Наиболее часто используют азот, как более доступный и дешевый. Газ-носитель обеспечивает перенос разделяемых компонентов по хроматографической колонке и не взаимодействует ни с разделяемыми веществами, ни с неподвижной фазой.
Одним из вариантов газовой хроматографии является газо-адсорбционная хроматография – это метод, в котором неподвижной фазой является твердый адсорбент. Разделение основано на различии в адсорбции на поверхности твердого носителя. Адсорбция может быть обусловлена неспецифическими (индукционными и дисперсионными) и специфическими взаимодействиями (комплексообразованием, либо образованием водородной связи) и зависит от природы адсорбента и сорбата. В качестве адсорбентов используют пористые носители, которые обладают химической, физической и термической стабильностью; однородной поверхностью, равномерным распределением по размеру пор и известной асорбционной активностью.. Достоинствами адсорбентов в качестве неподвижных фаз являются способность выдерживать высокие температуры, отсутствие фонового сигнала при работе с ионизационными детекторами и высокая селективность. Адсорбенты делятся на неорганические, полимерные (органические) и модифицированные. Среди неорганических адсорбентов особо важны сорбенты на основе углеродных материалов. Это неполярные сорбенты. Широко используются полярные неорганические сорбенты на основе двуокиси кремния. Особый интерес для газо-адсорбционной хроматографии представляет использование цеолитовых молекулярных
сит (M2/nO•Al2O3•xSiO2•yH2O).Наиболее многообразны полимерные сорбенты на основе пористых полимеров стирола и дивинилбензола. Основная область применения полимерных сорбентов – разделение полярных газов и высоко полярных органических соединений; определение воды в органических растворителях и летучих органических примесей в воде.
Классификация адсорбентов по их геометрической структуре:
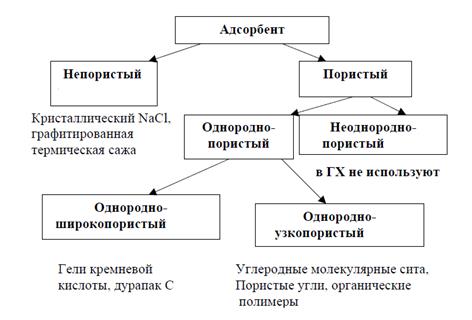
Газоадсорбционная хроматография является удобным методом определения в воздухе низких (до 0,03 мкг/л) таких токсичных газов, как фосфин и арсин. Возможно определение в воздухе таких токсичных и реакционно способных соединений, как Н2S, SO2, COS и меркаптанов. Газовая хроматография позволяет получать ценную и уникальную информацию о составе запахов пищевых продуктов, таких, как сыр, кофе, икра, коньяк и др. Газовая хроматография находит широкое применение в медицине для определения содержания многочисленных лекарственных препаратов, определения уровня жирных кислот, холестерина, стероидов и т.д. в организме больного. Успешно используется для определения содержания полициклических ароматических соединений, опасных для здоровья человека, в воде и в воздухе, уровня бензина в воздухе помещений автозаправочных станций, состава выхлопных газов автомобилей в воздухе и т.д.
Газо-жидкостная хроматография. В газо-жидкостной хроматографии разделение компонентов пробы достигается за счет многократного повторения процессов распределения между движущейся газовой и неподвижной жидкой фазами. Скорость миграции компонентов
зависит от их летучести и способности растворяться в стационарной жидкой фазе. Компоненты с низкой растворимостью в жидкой фазе и наибольшей летучестью при данной температуре продвигаются по колонке быстрее, и, наоборот, компоненты с низкой летучестью и высокой
растворимостью в стационарной фазе обладают малой подвижностью. Чем больше подвижность, тем меньше время удерживания. Этот вид хроматографии используется для разделения газов и паров жидкостей. В качестве адсорбентов используют стеклянные шарики,
силикагель и политетрафторэтилен.
Основное различие газо-жидкостной от газо-адсорбционной хроматографии заключается в том, что в первом случае метод основан на использовании процесса растворения и последующего испарения газа из жидкой пленки, удерживаемой твердым инертным носителем; во втором случае процесс разделения основан на адсорбции и последующей десорбции газа или пара на поверхности твердого вещества – адсорбента. В газо-жидкостной хроматографии применяется ряд детекторов, специфически реагирующих на любые органические вещества. К их числу относятся ионизационные детекторы, детекторы электронного захвата, термоионные, спектрофотометрические и некоторые другие детекторы.
Метод применяется для определения широкого круга соединений в атмосферном воздухе и воздухе жилых и производственных помещений, различных водах и почве. Наиболее важными классами определяемых соединений являются нефтепродукты, диоксины, полихлоринованные бифенилы, амины, полициклические ароматические углеводороды и пестициды.
Прибор. Принципиальная схема газового хроматографа:

1- баллон с газом-носителем; 2- блок подготовки газов; 3- дозирующая петля; 4- испаритель; 5- колонка; 6-термостат; 7- детектор; 8 – блок питания; 9- усилитель сигнала детектора; 10- регистрирующее устройство.
В данном приборе имеется система подачи потока газа-носителя, система подготовки и ввода исследуемой смеси, хроматографическая колонка с системой регулирования ее температуры, анализирующая система (детектор) и система регистрации результатов разделения и анализа (регистратор).
Разделение в хроматографической колонке является важнейшей операцией всего процесса газохроматографического анализа. Вышедшие из колонки бинарные смеси (газ-носитель – компонент) попадают в детектирующее устройство, где происходит преобразование изменений концентраций компонентов во времени в электрический сигнал, регистрируемый при помощи специальной системы в виде кривой, называемой хроматограммой. Результаты всего опыта в значительной степени зависят от правильного выбора типа детектора, его конструкции. Существует несколько классификаций детекторов. Различают дифференциальные и интегральные детекторы. Дифференциальные детекторы регистрируют мгновенное значение одной из характеристик (концентрации или потока) во времени. Интегральные детекторы суммируют количество вещества за определенный промежуток времени. Также применяют разнообразные по принципу действия, чувствительности и назначению детекторы: термокондуктометрические, ионизационные, спектроскопические, масс-спектрометрические, кулонометрические и многие другие.
Универсальным является катарометр – детектор по теплопроводности, принцип работы которого основан на изменениитемпературы нагретых нитей (чувствительных элементов) в зависимостиот теплопроводности окружающего газа, которая определяется егосоставом. Детектор измеряет различие в теплопроводности чистого газа-носителя и смеси газа-носителя с определяемым веществом. Наиболее широко используются ионизационные детекторы,
принцип работы которых основан на изменении ионного тока, вызванного введением в детектор анализируемого вещества. Ионный ток возникает под действием источника ионизации и электрического поля между электродами детектора. В качестве источников ионизации используют: – пламена (пламенно-ионизационный детектор), – электронную и ионную эмиссию (термоионный детектор), – радиоактивные изотопы (детектор электронного захвата)
– электрический разряд, – фотоионизацию (фотоионизационный детектор).
Жидкостная хроматография.
Жидкостная хроматография (ЖХ) - метод разделения и анализа сложных смесей веществ, в котором подвижной фазой является жидкость. Подвижная фаза в жидкостной хроматографии выполняет двоякую функцию: 1) обеспечивает перенос десорбированных молекул по колонке
(подобно подвижной фазе в газовой хроматографии); 2) регулирует константы равновесия, а, следовательно, и удерживание в результате взаимодействия с неподвижной фазой (сорбируясь на поверхности) и с молекулами разделяемых веществ.
Высокоэффективная жидкостная хроматография. Этоодин из эффективных методов анализа и разделения сложных смесей. Широкое применение этого метода связано с большим диапазоном молекулярных масс веществ, с которыми можно работать: от нескольких единиц до десятков миллионов. По механизму разделения анализируемых или разделяемых веществ ВЭЖХ делится на адсорбционную, распределительную, ионообменную и эксклюзионную.
Одним из вариантов жидкостной хроматографии является жидкостно-адсорбционная хроматография – это метод, в котором неподвижной фазой является твердый адсорбент. В адсорбционной хроматографии разделение осуществляется за счет разницы в адсорбируемости молекул, проходящих через слой частиц сорбента, покрытых неподвижной фазой в виде тонкого слоя
Последнее изменение этой страницы: 2016-08-11
lectmania.ru. Все права принадлежат авторам данных материалов. В случае нарушения авторского права напишите нам сюда...