
Категории:
ДомЗдоровьеЗоологияИнформатикаИскусствоИскусствоКомпьютерыКулинарияМаркетингМатематикаМедицинаМенеджментОбразованиеПедагогикаПитомцыПрограммированиеПроизводствоПромышленностьПсихологияРазноеРелигияСоциологияСпортСтатистикаТранспортФизикаФилософияФинансыХимияХоббиЭкологияЭкономикаЭлектроника
Газовые смеси Давление газовых смесей.
Парциальные давления газов. Закон Дальтона.
Уравнение состояния идеального газа относится не только к индивидуальному газу, но также применимо и к смесям газов в любой пропорции, при условии, что газы при смешении не взаимодействуют между собой.
Закон Дальтона: «Общее давление смеси газов, находящихся в определённом объёме, равно сумме парциальных давлений  всех входящих в него газов», т.е.
всех входящих в него газов», т.е.

где  – общее давление газовой смеси;
– общее давление газовой смеси; 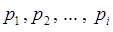 – парциальные давления компонентов газовой смеси.
– парциальные давления компонентов газовой смеси.
Парциальное давление – это то давление, которое бы создавал каждый газ, входящий в состав газовой смеси на стенки сосуда, как если бы  -й газ занимал весь объём смеси при одной и той же температуре и отсутствии других газов.
-й газ занимал весь объём смеси при одной и той же температуре и отсутствии других газов.
Если газовая смесь содержит  число молей компонентов (газов), то очевидно общее число молей будет равно:
число молей компонентов (газов), то очевидно общее число молей будет равно:
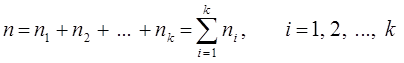
Пусть общий объём смеси, занимаемый при температуре  , будет равен
, будет равен  , тогда очевидно, что для парциальных давлений
, тогда очевидно, что для парциальных давлений 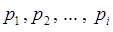 этих компонентов в смеси должны быть справедливы следующие соотношения вида:
этих компонентов в смеси должны быть справедливы следующие соотношения вида:

откуда следует, что:

тогда будем иметь соответственно:

откуда:

или в окончательном виде:

поскольку:

тогда:

Итак, в ходе проделанных выкладок мы пришли к следующим двум уравнениям:

Деля уравнение (1) на уравнение (2), будем иметь соответственно:

и таким образом имеем:

откуда следует, что:

Введём понятие мольной доли. По определению имеем:

где  – мольная доля газа (компонента) газовой смеси и таким образом из полученного нами уже выше выражения вида:
– мольная доля газа (компонента) газовой смеси и таким образом из полученного нами уже выше выражения вида:

будем иметь соответственно:

Взаимосвязь величин, входящих в уравнение состояния.
Цепочечное соотношение Эйлера.
Как было выяснено нами уже в предыдущих разделах, физическое состояние идеального газа, определяется тремя величинами – температурой, давлением и объёмом. Все эти величины находятся между собой в определённой функциональной зависимости и выражаемой уравнением состояния вида:
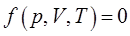
Параметры, входящие в уравнение состояния, в свою очередь также связаны, находясь в функциональной зависимости между собой. Несмотря на явную взаимосвязь величин входящих в уравнение состояния, наибольшей наглядностью обладает так называемое цепочечное соотношение Эйлера, показывающее функциональную зависимость величин, входящих в уравнение состояния. Для вывода такого уравнения, рассмотрим процессы, протекающие при постоянной температуре, давлении и объёме.
А. Изотермический процесс.
Здесь по определению:

а также:

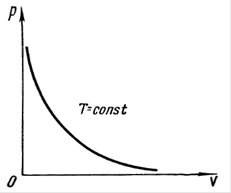
Рис.5. Изотерма идеального газа в координатах 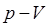
Учитывая, что:

имеем:

Тогда соответственно:

и таким образом:

откуда следует, что:

и далее имеем соответственно:
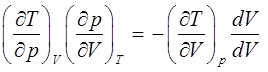
откуда:

откуда:
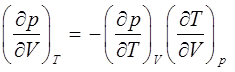
Б. Изобарический процесс.
Здесь по определению:

а также:


Рис.6. Изобара идеального газа в координатах 
Учитывая, что:

имеем:

Тогда соответственно:

и таким образом:

откуда следует, что:

и далее имеем соответственно:

откуда:

откуда:

В. Изохорический процесс.
Здесь по определению:

а также:


Рис.7. Изохора идеального газа в координатах 
Учитывая, что:

имеем:

Тогда соответственно:

и таким образом:

откуда следует, что:
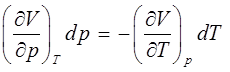
и далее имеем соответственно:

откуда:

откуда:

Таким образом, в ходе проделанных выкладок, мы пришли к трём взаимно эквивалентным уравнениям:

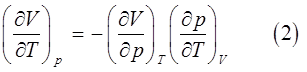

соответственно для изотермического (1), изобарического (2) и изохорического (3) процессов. Выбрав любое из полученных нами выше уравнений, путём алгебраических преобразований можно получить так называемое цепочечное соотношение Эйлера, увязывающее между собой параметры состояния идеального газа в уравнении состояния. Так, имеем соответственно:
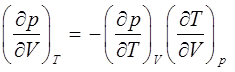
откуда:

откуда:

откуда:

и в окончательном виде:

Полученное выше соотношение носит название цепочечное соотношение Эйлера. Данное соотношение увязывает между собой параметры состояния – совокупность внешних и внутренних переменных идеального газа в уравнении состояния.
Последнее изменение этой страницы: 2016-08-11
lectmania.ru. Все права принадлежат авторам данных материалов. В случае нарушения авторского права напишите нам сюда...