
Категории:
ДомЗдоровьеЗоологияИнформатикаИскусствоИскусствоКомпьютерыКулинарияМаркетингМатематикаМедицинаМенеджментОбразованиеПедагогикаПитомцыПрограммированиеПроизводствоПромышленностьПсихологияРазноеРелигияСоциологияСпортСтатистикаТранспортФизикаФилософияФинансыХимияХоббиЭкологияЭкономикаЭлектроника
Термодинамика электрохимических систем и электродных процессов. Условная водородная шкала. Правило знаков ЭДС и электродных потенциалов. Электрохимический потенциал. Электрохимические равновесия
Пусть в электрохимической системе обратимо и изотермически протекает процесс:
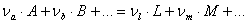 (1.1.1)
(1.1.1)
Работа по перемещению электрического заряда равна:
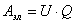 (1.1.2)
(1.1.2)
Для обратимой реакции:
 (1.1.3)
(1.1.3)
Полезная работа обратимого процесса максимальна и равна убыли изобарного потенциала системы, т. е:
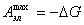 (1.1.4) при p,T=const
(1.1.4) при p,T=const
Изменение изобарного потенциала вызвано совокупностью электрохимических реакций на электродах, т. Е. суммарной химической реакцией или другими физико-химическими процессами (растворение, выравнивание концентраций, фазовое превращение и др.).
С учетом того, что U=E и  , и формул (1.1.2), (1.1.3) и (1.1.4), получаем:
, и формул (1.1.2), (1.1.3) и (1.1.4), получаем:
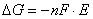 (1.1.5)
(1.1.5)
Производная ΔG по температуре:
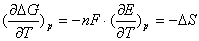 (1.1.6)
(1.1.6)
Таким образом, измерив ЭДС системы и ее температурный коэффициент, можно легко найти величины ΔG и ΔS для суммарного процесса, протекающего в электрохимической системе. Этот процесс является самопроизвольным, следовательно, ΔG < 0.
Важную термодинамическую характеристику этого процесса – изменение энтальпии – вычисляют по уравнению Гиббса – Гельмгольца.
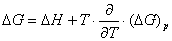 (1.1.7)
(1.1.7)
 (1.8)
(1.8)
ЭДС электрохимической системы находят по уравнению:
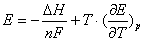 (1.9)
(1.9)
Чтобы связать ЭДС с константой равновесии, используют изотерму Вант – Гоффа. Если предположить, что реакция (1.1.1) протекает в жидком растворе, то:
 (1.1.10)
(1.1.10)
С учетом (1.1.5) и (1.1.10) получается:
 (1.1.11)
(1.1.11)
При 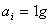 получаем
получаем  , где
, где 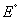 - это стандартная величина ЭДС системы.
- это стандартная величина ЭДС системы.
С учетом этого получают общее выражение ЭДС электрохимической цепи или уравнение Нернста:
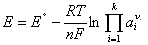 (1.1.12)
(1.1.12)
Приведенные выше уравнения дают возможность вычислить величины ΔG и К по экспериментальным значениям Е и, наоборот, рассчитать Е, зная термодинамические характеристики химической реакции.
Таким образом, измерение ЭДС электрохимических элементов и цепей является очень простым и точным методом вычисления термодинамических характеристик химических реакций и некоторых важных физико-химических процессов в растворах. Нельзя забывать, что этот метод подходит только для тех случаев, когда процесс в электрохимической системе обратим.
В связи с тем, что в настоящее время нет прямых экспериментальных и расчетных методов определения отдельных скачков потенциала на границе раздела фаз в гальваническом элементе, значение потенциала отдельных электродов приводят относительно потенциала какого-либо стандартного электрода, потенциал которого условно принимают равным 0 при любых температурах. Таким стандартным электродом, или электродом сравнения, является обратимый водородный электрод, в котором газообразный водород находится при давлении 1 атм. и насыщает платиновый электрод. Раствор, в который погружен водородный электрод, содержит ионы водорода (гидроксония), причем активность H+ равна единице.
Согласно Международной конвенции (1953 г.), электродным потенциалом электрода называется ЭДС элемента, составленного из этого электрода (справа) и стандартного водородного электрода (слева).
Например, для нахождения электродного потенциала цинка составляют элемент
(+) Pt, H2│H+, aq║Zn2+, aq│Zn (–) [1].
Пусть на границе электрод – раствор в результате протекания процессов с участием заряженных и незаряженных частиц устанавливается равновесие, описываемое уравнением (1.1).
Рассмотрим два примера установления электрохимического равновесия на границе раздела фаз.
1. Граница двух различных металлов.
При установлении равновесия на этой границе происходит выравнивание электрохимических потенциалов электронов в металлах М1 и М2.
Условие равновесия имеет вид
 (1.1.13)
(1.1.13)
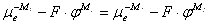 (1.1.14)
(1.1.14)
Отсюда для гальвани-потенциала на границе металл – металл получают выражение:
 (1.1.15)
(1.1.15)
Таким образом, в условиях равновесия работа перенесения электрона из одного металла в другой равна нулю, но работа переноса единицы воображаемого заряда, т. е.  , отлична от нуля, поскольку химические потенциалы электрона в различных металлах неодинаковы.
, отлична от нуля, поскольку химические потенциалы электрона в различных металлах неодинаковы.
2. Граница металла М с раствором, содержащим ионы этого же металла. При установлении равновесия происходит выравнивание электрохимических потенциалов ионов Mz+ в растворе и в кристаллической решетке металла.
При равновесии:
 (1.1.16)
(1.1.16)
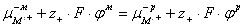 (1.1.17)
(1.1.17)
Гальвани-потенциал на границе металл – раствор соответствующей соли имеет вид:
 (1.1.18)
(1.1.18)
Поскольку 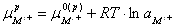 , а
, а  , уравнение (1.1.18) можно переписать в виде:
, уравнение (1.1.18) можно переписать в виде:
 (1.1.19)
(1.1.19)
Уравнение (1.1.19) – это частный случай уравнения Нернста для отдельного гальвани-потенциала. Таким образом, в условиях рассмотренного электрохимического равновесия работа перенесения иона Mz+ из металла в раствор или обратно равна нулю. Гальвани-петенциал 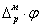 зависит от концентрации потенциалопределяющих ионов Mz+ и также может быть сведен к нулю. Однако невозможность измерить гальвани-потенциал не позволяет установить, при какой именно концентрации Mz+
зависит от концентрации потенциалопределяющих ионов Mz+ и также может быть сведен к нулю. Однако невозможность измерить гальвани-потенциал не позволяет установить, при какой именно концентрации Mz+ 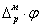 =0.
=0.
Правильно разомкнутая электрохимическая цепь, на концах которой можно измерить электрическую разность потенциалов, всегда должна заканчиваться одинаковыми по своему химическому составу металлами. Электрохимическая цепь является равновесной при условии, что электрохимическое равновесие наблюдается на каждой фазовой границе, а разность потенциалов на концах цепи Е скомпенсирована разностью потенциалов от внешнего источника цепи.
Из (1.1.5):
E=–ΔG/nF (1.1.20)
Т.е. разность потенциалов на концах равновесной электрохимической цепи однозначно связана с изменением свободной энергии Гиббса в ходе соответствующей химической реакции. Величина E и называется ЭДС, т.е. электродвижущей силой электрохимической цепи. Уравнение (1.1.20) применимо только в том случае, если на всех фазовых границах устанавливается равновесие, в противном случае разность потенциалов на концах цепи не равна ЭДС и уравнение оказывается неприменимым [2].
Последнее изменение этой страницы: 2016-08-11
lectmania.ru. Все права принадлежат авторам данных материалов. В случае нарушения авторского права напишите нам сюда...