
Категории:
ДомЗдоровьеЗоологияИнформатикаИскусствоИскусствоКомпьютерыКулинарияМаркетингМатематикаМедицинаМенеджментОбразованиеПедагогикаПитомцыПрограммированиеПроизводствоПромышленностьПсихологияРазноеРелигияСоциологияСпортСтатистикаТранспортФизикаФилософияФинансыХимияХоббиЭкологияЭкономикаЭлектроника
Механический и магнитный моменты атома. LS-связь.
Различают два способа расчёта суммарного момента атома ls-связь и jj-связь
Под ls связью понимают случай когда орбитальные моменты всех электронов в атоме связаны между собой сильнее чем орбитальные и спиновой момент каждого элуктрона в отдельности
Аналогично спиновые моменты всех электронов связаны между собой прочнее, чем с орбитальным моментом каждого электроа
При jj-связи связь между орбитальным и спиновым моментом бля каждого электрона сильнее, чем связь с орбит (спинов) моментом друг электр. В ls-связи расчитыв с учётом правил. квантов. сначал полный орбит и спи моменты, а затем полн. мех. момент атома.
Для ls-связи необходимо рассчитать сумм орбит и сумм спинов момент атома запишем углов квантов орбит момента импульса
M2=ħ2L(L+1)
Квантовое число L для 2-ух электронов принимает значение от l1 до | l2-l1|
(L=l1+l2; l1+l2-1; | l2-l1|)
Добавим 3-ий электрон в этом случае число (L) меняется
(L=l1+l2+l3; l1+l2+l3-1; lmin)
lmin – минимальное значение по-парной суммы квантового числа для 2-ух электронов с третьим квантовым числом l3
Пример
(l1=1; l2=2; l3=2)
1) L12=2 -
2) L12=1 - добавляем l3=2
3) L12=0 -
Получаем
1) L123=4;3;2;1;0 -
2) L123=3;2;1 - для трёх электронов получаем
3) L12=2 - L=4;3;2;1;0
Для проекции орбитального момента атома
Mz=ml ħ ( Mz=m ħ)
(ml=-L; -L+1;…..0…L;)
Для суммарного спинового момента атома
Mz2= ħ2S(S+1)
Квантов число (для 2-ух электронов)
(S=S1+S2;…;|S1-S2|)
Для н-го колич электронов возможно 2 случ
-если в атоме чётное число электронов, то число S будет меньше(Nx1/a,0)
-при нечетном количестве электронов спиновое число будет полуцелым, то будет менье (Nx1/2…;1/2)
Полный мех момент атома J, определяется
Mj2= ħ2j(j+1)
(j=L+S…|L-S|)
Условие квантов
Mjz= ħ
(Mj=-J; -J+1;.. 0.. J)
27 Понятия об энергетических уровнях молекул. 
a,b- яра(+)
1б2-электроны (-)
Для молекул водорода ур Шредингера имеет вид
()+(E- Ub3)=0
Ub3=1/4πε0(e2/rab+e2/r12-e2/ra1-e2/ra2-e2/rb1- e2/rb2)
Данное уравнение Шредингера имеет 2 решения для собственных значений, котор получ в случае различной ориент спинов электронов.
Молекула водорода образуются только в том случае если спины электр атома водорода направлены в против стороны
r0- соотв стабильному состоянию молекулы
Е0- энергия диссоциации молекулы (такая модекула нужна чтобы разрушить молекулу) 
Помимо энергии обусловл электр которыми молекула может обладать ещё 2-мя вид энергии: колеб и вращательными

Е=Еэл +Еколеб + Ерот
(виб) (вращ)
Еэл=-R z2/n2 n=1,2,3….(атом водорода)
z – зарядовое число (кол протонов в ядр)
Еколеб=(ν+1/2)ħω ν=0,1,2
(квантовый гармон асуллятор)
Выражение для вращ энергии получим из следующего выражения были форм из классич мех
I- момент энерции
Евращ= Iω2/2=I2ω2/2I
Iω=M
Eвращ=M2/2I применение условие квантован квадрата момента импульса
Евращ=ħ2 j (j+1)/2I j=0,1,2
E=-R z2/n2 + (ν+1/2)ħω+ħ2j(j+1)/2I
На квантов число j и ν накл правила отбора Δy=±1; Δν±1
28.Рентгеновские спектры. Закон Мозли. 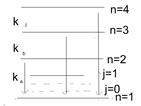
Рентгеновское излучение называю ещё характеристич излучением, т.к. по рентгеновским спектрам определяет порядок номер элемент в табл Менделеева
Р спектры возник тогда, когда с внутр оболочек атомов вырывается электрон, образуется вокантное место, на которое переходят электроны с более высоких энергетич уровней. В зависимости от того с какой оболочки выбит электрон в характерист излучении выдел серии k,l,M,N
Мозли установил закон связыв частоту рентген излуч с поряд номером эл в таблице Менделевва
ω=R(z-δ)2(1/n12-1/n22)
z- порядковый номер таблицы Менделев
δ- поправка учитыв экранир действий электронов находящих вблизи ядра
n1 – номер уровня на который переходит электрон
n2 – с которого переходит лектрон
Закон Мозли в сокращ виде записыв
=c(z-δ)
Характер излучен можно рассмотреть как излучение возникшее при переходе электрона с одного уровня на другой, как излучение возникающее в атоме
Основная проблема при злучени рентген спектров это опред поправки δ, которая различна при переходе с различных уровней.
Принцип тождества микрочастиц
В квантовой механике в ансамбле одинаковых частиц невозможно отличить одну частицу от другой.

В квантовой механике свободной частице можно сопоставить групповой пакет. Групповой пакет со временем размывается. В закрытых областях оба пакета перекрылись. В ней не возможно отличить одну группу от другой.

Во 2-ом примере невозможно ответить с точки зрения квантовой механики, где находиться каждая из указанных частиц.
Рассмотрим ансамбль из n одинаковых частиц, координаты которых обозначим через qi.
Зафиксируем некоторые составляющие ансамбля n, опишем его волновой функцией:
Ψ(…, qi, qk,…)
Подействуем на волновую функцию оператором перестановки:
Ψ(…, qi, qk,…)=Ψ(…, qk, qi,…) (1)
Действие оператора на собственную волновую функцию сводится к умножению собственного значения оператора на собственную волновую функцию:
Ψ(…, qi, qk,…)=λΨ(…, qi, qk,…) (2)
Подействуем еще раз оператором перестановки на выражения (1) и (2):
Ψ(…, qi, qk,…)=Ψ(…, qk, qi,…)
Ψ(…, qi, qk,…)=Ψ(…, qi, qk,…) (3)
Ψ(…, qi, qk,…)=λΨ(…, qi, qk,…)
Ψ(…, qi, qk,…)=λΨ(…, qi, qk,…) (4)
Сравним уравнения (3) и (4), след. =1
Для нахождения собственного значения
λ=±1
Вернемся к выражению (2)
Существуют такие ансамбли одинаков частиц, которые опис волновыми функциями меняющими свой знак при перестановке частиц т.е
Ψ(…, qi, qk,…)=-Ψ(…, qi, qk,…)
Такие функции называются нечетными или несиметричными и описывают частицы с полуцелым спином.
Частицы, имеющие полуцелый спин, называются фермионами. Подчиняются статистике Ферми-Дирака.
Существуют такие частицы, при перестановке которых, волновая функция, описывающая состояние из системы таких частиц, не меняется:
Ψ(…, qi, qk,…)=Ψ(…, qi, qk,…)
Такие функции называются четными или симметричными, они описывают частицы с целым спином.
Типичным представителем частицы с целым спином является фотон.
Частицы с целочисленным спином называются бозонами. Подчиняются статистике Бозе-Эйнштейна.
Поведение фермионов принимают отличным от поведения бозонов.
Фермионы – частицы, подчиняющиеся принципу Паули (в состоянии описываемом четверкой квантовых чисел (n, l, m, ms) может находится только один электрон).
Бозон – коллективистская частица – чем больше бозонов находится в каком-либо состоянии, тем больше вероятность, что и другие бозоны окажутся в этом состоянии.
Последнее изменение этой страницы: 2016-08-11
lectmania.ru. Все права принадлежат авторам данных материалов. В случае нарушения авторского права напишите нам сюда...