
Купить тушенку ГОСТ оптом Крупнокусковая тушенка оптом от завода! Высший сорт, выгодные цены!
Категории:
ДомЗдоровьеЗоологияИнформатикаИскусствоИскусствоКомпьютерыКулинарияМаркетингМатематикаМедицинаМенеджментОбразованиеПедагогикаПитомцыПрограммированиеПроизводствоПромышленностьПсихологияРазноеРелигияСоциологияСпортСтатистикаТранспортФизикаФилософияФинансыХимияХоббиЭкологияЭкономикаЭлектроника
Молекула оксида углерода (II) СО
 |
Между атомами углерода и кислорода образуются 3 связи:
■ две по обменному механизму и
■ одна по донорно-акцепторному механизму:
«O» - донор, «C»- акцептор.
3 ковалентные связи образуются за счет перекрывания 3-х р-АО каждого атома.
Структура молекулы – линейная.

Одна связь -s связь, а две другие - p -связи:
|
Связь называется - p - связь:
Перекрывание АО при образовании p-связей меньше (Есв-меньше), чем при s-связях, поэтому p -связи менее прочные.
Молекула Н2S

структура – угловая, валентный угол – 92о
▓ Почему валентный угол в ряду молекул:
H2S (92o), Н2Se (91o) и Н2Те (89о) изменяется?
S, Se и Te - электронные аналоги : S ¼3s23р4
Se ¼4s24p4
Te ¼5s25p4
Пространственная конфигурация всех молекул – угловая. Причина изменения валентного угла:
Þ увеличение размера атома;
Þ увеличеие расстояния между связывающими
электронными парами;
Þ уменьшение силы отталкивания между ними;
Þ уменьшение валентного угла.

Молекула НСl:
ЭО(Cl) = 3,0 ЭО(Н) = 2,1
Þ связывающая электронная пара смещена в сторону Cl: Þ эффективный отрицательный заряд (-q) у атома Cl
эффективный положительный заряд (+q) у атома Н
Þ электрический диполь.
|
 |
электрический момент диполя связи mсв
|
mсв некоторых связей
 |
| молекула | DЭО | mсв×10-30,Кл×м | Вывод |
| Н – Сl | 0,90 | 1,03 | Чем больше DЭО, тем больше mсв и, следовательно, связь более полярная |
| Н – Br | 0,74 | 0,78 | |
| H - I | 0,40 | 0,38 |
 | |||
|
Электрический момент
диполя молекулы (mм)
Полярность молекулы зависит от ее геометрической структуры.
2-х атомные молекулы Þ линейная структура Þ mм =mсв
|
Молекула Н2S
Þугловая структура ( Ð920)
ЭО(Н) = 2,1 и ЭО(S) = 2,5 Þ связь полярная.

mм = Smсв¹ 0 Þ молекула в целом полярная.
Молекула SbН3
 Sb…5s25p3
Sb…5s25p3
|

Н 1s1 Н 1s1 Н 1s1

Гибридизация:
|
Если у атома в образовании химических связей участвуют разные по типу АО (s-, p-, d- или f-АО), то химические связи формируются электронами не «чистых», а «смешанных», или гибридных орбиталей.
Перекрывание гибридных АО происходит в большей степени, чем негибридных орбиталей Þ
► химические связи прочнее
► молекула более устойчива.
Гибридная орбиталь:
 |
Типы гибридизации АО и структура молекул

| Орбитали, участвующие в гибридизации | Тип гибридизации | Структура молекулы | Валентный угол |
| s +p | sp |  Линейная
Линейная
| 180о |
| s+p+p | sp2 |  плоский треугольник
плоский треугольник
| 120о |
| s+p+p+p | sp3 |  тетраэдр
тетраэдр
| 109,3о |
Молекула ВеСl2

■ sp-гибридизация АО Ве , Ð180о
■ пространственная структура Þ линейная.

Cl Be Cl
■ связь полярная m св ¹ 0,т.к. ЭО Ве и Cl: 1,5 и 3,0
Þ Cl Be ® Cl
■ mмол = Smсв = 0 Þ молекула в целом неполярная.
Молекула ВН3
 |
В* 2s1 2p2
H 1s H 1s H 1s
■ s-s перекрывание и два p-s перекрывания АО.
■ sp2–гибридизация 
АО В
■ 3 s - связи, Ð 120° ,
■ связи полярные DЭО = (2.1-2.0) ¹ 0.
■ структура молекулы - плоский треугольник.
■ mмол = Smсв = 0 Þ молекула ВН3 - неполярная.
Молекула SiCl4
Si* 3s 3pCl 3s 3p
 |
Cl 3s 3p Cl 3s 3p Cl 3s 3p
■ 1 s-АО и 3 р-АО Þ sp3- гибридизацияАО
■ структура молекулы Þ тетраэдр,Ð 109,30

■ Smсв= 0 - молекула в целом неполярная.
►Вывод:
 |
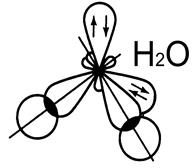
Молекулы NН3 и Н2О
 N…2s22p3 O…2s22p4
N…2s22p3 O…2s22p4
 |
H 1s1 H 1s1 H1s1 Н 1s1 Н 1s1
Структура молекул – тетраэдр. Метод ВС не объясняет структуру молекул, определенную методомрентгеноструктурного анализа
sp3 – гибридизация АО азота «N» и кислорода «О».

Последнее изменение этой страницы: 2016-08-11
lectmania.ru. Все права принадлежат авторам данных материалов. В случае нарушения авторского права напишите нам сюда...

