
Категории:
ДомЗдоровьеЗоологияИнформатикаИскусствоИскусствоКомпьютерыКулинарияМаркетингМатематикаМедицинаМенеджментОбразованиеПедагогикаПитомцыПрограммированиеПроизводствоПромышленностьПсихологияРазноеРелигияСоциологияСпортСтатистикаТранспортФизикаФилософияФинансыХимияХоббиЭкологияЭкономикаЭлектроника
Порядок реакции. Вывод и анализ кинетического уравнения первого порядка.
Для того, чтобы записать кинетическое уравнение, необходимо экспериментально определить величину константы скорости и показателей степени при концентрациях реагирующих веществ. Показатель степени при концентрации каждого из реагирующих веществ в кинетическом уравнении химической реакции есть частный порядок реакции по данному компоненту. Сумма показателей степени в кинетическом уравнении химической реакции представляет собой общий порядок реакции. Стехиометрическое уравнение реакции представляет собой уравнение материального баланса и никоим образом не может определять характера протекания этой реакции во времени.
В химической кинетике принято классифицировать реакции по величине общего порядка реакции. Рассмотрим зависимость концентрации реагирующих веществ от времени для необратимых (односторонних) реакций нулевого, первого и второго порядков.
Рассмотрим зависимость от времени концентрации исходного вещества А для случая реакции первого порядка А ––> В. Реакции первого порядка характеризуются кинетическим уравнением вида:


После интегрирования выражения получаем:

Константу интегрирования g определим из начальных условий: в момент времени t = 0 концентрация С равна начальной концентрации Со. Отсюда следует, что g = ln Со. Получаем:


Т.о., логарифм концентрации для реакции первого порядка линейно зависит от времени и константа скорости численно равна тангенсу угла наклона прямой к оси времени.
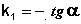
Из уравнения (II.9) легко получить выражение для константы скорости односторонней реакции первого порядка:

Еще одной кинетической характеристикой реакции является период полупревращения t1/2 – время, за которое концентрация исходного вещества уменьшается вдвое по сравнению с исходной. Выразим t1/2 для реакции первого порядка, учитывая, что С = ½Со:

Отсюда

как видно из полученного выражения, период полупревращения реакции первого порядка не зависит от начальной концентрации исходного вещества.
Общие положения и закономерности катализа.
Катализ – явление изменения скорости химической реакции в присутствии веществ, состояние и количество которых после реакции остаются неизменными.
Вещество, входящее в структуру активированного комплекса, но стехиометрически не являющееся реагентом, называется катализатором. Для всех катализаторов характерны такие общие свойства, как специфичность и селективность действия.
Специфичность катализатора заключается в его способности ускорять только одну реакцию или группу однотипных реакций и не влиять на скорость других реакций. Так, например, многие переходные металлы (платина, медь, никель, железо и т.д.) являются катализаторами для процессов гидрирования; оксид алюминия катализирует реакции гидратации и т.д.
Селективность катализатора – способность ускорять одну из возможных при данных условиях параллельных реакций. Благодаря этому можно, применяя различные катализаторы, из одних и тех же исходных веществ получать различные продукты:
[Cu]: СО + Н2 ––> СН3ОН
[Al2О3]: С2Н5ОН ––> С2Н4 + Н2О
[Ni]: СО + Н2 ––> СН4 + Н2О
[Cu]: С2Н5ОН ––> СН3СНО + Н2
Причиной увеличения скорости реакции при положительном катализе является уменьшение энергии активации при протекании реакции через активированный комплекс с участием катализатора.
Если предположить, что предэкспоненциальные множители в уравнении Аррениуса для каталитической и некаталитической реакций близки, то для отношения констант скорости можно записать:

Если ΔEA = –50 кДж/моль, то отношение констант скоростей составит 2,7·106 раз (действительно, на практике такое уменьшение EA увеличивает скорость реакции приблизительно в 105 раз).
Необходимо отметить, что наличие катализатора не влияет на величину изменения термодинамического потенциала в результате процесса и, следовательно, никакой катализатор не может сделать возможным самопроизвольное протекание термодинамически невозможного процесса (процесса, ΔG (ΔF) которого больше нуля). Катализатор не изменяет величину константы равновесия для обратимых реакций; влияние катализатора в этом случае заключается только в ускорении достижения равновесного состояния.
В зависимости от фазового состояния реагентов и катализатора различают гомогенный и гетерогенный катализ.

Энергетическая диаграмма химической реакции без катализатора (1)
и в присутствии катализатора (2).
6. Определите степень электролитической диссоциации фтористоводородной кислоты в 0,1 М растворе. Константа диссоциации кислоты равна 7,4∙10-4.

7. Рассчитайте молярную электрическую проводимость при бесконечно большом разбавлении для LiBr, если λ∞(KBr) = 151,9; λ∞(K2SO4) = 153,3; λ∞( Li2SO4) = 118,5 Ом-1∙см2.
λ∞(KBr) = λK+ + λBr- = 151,9 (1)
λ∞(K2SO4) = λK+ + λ(SO42-) = 153,3 (2)
λ∞(Li2SO4) = λLi+ + λ(SO42-) = 118,5 (3)
Для получения выражения
λ∞(LiBr) = λLi+ + λBr- надо вычесть (3) –(2) и добавить (1):
λ∞(LiBr) = λLi+ + λBr- = 118.5 – 153.2 +151.9 = 117.2
8. Вычислите константу равновесия реакции 2KBr + Cl2 = 2KCl + Br2 при 250С, если
Cl2 + 2e- = 2Cl-, φ01 = 1,36 В
Br2 + 2e- = 2Br-, φ02 =1,09 В.
ЭДС=Еок-Евосст.=1,36-1,09=0,27
lnKa=z*F*ЭДС/R*T=2*96500*0,27/8,314*298=21,03
Ка=1,36*109
9. Элемент состоит из водородного электрода, погруженного в желудочный сок с неизвестной концентрацией водородных ионов, и каломельного электрода с насыщенным раствором КCl. Определите рН и С (Н+) желудочного сока, если ЭДС элемента при 180 С 0,33 В. φ 18 калом. насыщ.= 0,2438 В.
рН= 1*(Е-Екал)/2,303b0=1*(0,33-0,2438)/2,303*0,025=1,56
b0=R*T/F=8,314*(273+18)/96500=0,025
С (Н+) = 10-pH= 0.027
Последнее изменение этой страницы: 2016-08-11
lectmania.ru. Все права принадлежат авторам данных материалов. В случае нарушения авторского права напишите нам сюда...