
Категории:
ДомЗдоровьеЗоологияИнформатикаИскусствоИскусствоКомпьютерыКулинарияМаркетингМатематикаМедицинаМенеджментОбразованиеПедагогикаПитомцыПрограммированиеПроизводствоПромышленностьПсихологияРазноеРелигияСоциологияСпортСтатистикаТранспортФизикаФилософияФинансыХимияХоббиЭкологияЭкономикаЭлектроника
ОБЩИЕ СВЕДЕНИЯ О ФЛОТАЦИОННОМ РАЗДЕЛЕНИИ МИНЕРАЛОВ
ОБЩИЕ СВЕДЕНИЯ О ФЛОТАЦИОННОМ РАЗДЕЛЕНИИ МИНЕРАЛОВ
Флотация – процесс разделения тонкоизмельченных полезных ископаемых, осуществляемый в водной среде и основанный на различии их способности, естественной или искусственно создаваемой, смачиваться водой, что определяет избирательное прилипание частиц минералов к поверхности двух фаз.
Флотационный процесс осуществляется чаще всего в трехфазной системе, включающей твердую, жидкую и газообразную фазы.
Из всех разновидностей флотационного процесса наиболее широкое распространение получила пенная флотация, которая основана на способности несмачиваемых (гидрофобных) минералам прилипать к пузырькам воздуха, образующимся в результате аэрации пульпы, и всплывать вместе с ними на поверхность, образуя пенный продукт. Смачиваемые же (гидрофильные) минералы остаются взвешенными в пульпе, образуя камерный продукт.
Минеральные частицы, закрепившиеся на поверхности воздушных пузырьков, называются флотирующимися, незакрепившиеся – нефлотирующимися.
Крупность флотируемых частиц в процессе пенной флотации обычно не превышает 0,15мм. Для углей и калийных солей эта крупность может быть увеличена до 0,5мм.
Для увеличения естественного различия смачиваемости поверхности минералов или для искусственного создания такого различия минеральную поверхность обрабатывают специальными веществами, называемыми флотационными реагентами. С помощью подбора флотационных реагентов можно достигнуть условий, при которых одни минералы будут флотироваться, а другие – нет, т.е. создать условия для селективного их разделения.
В настоящее время флотация широко применяется для обогащения большинства руд цветных и редких металлов, апатитовых, фосфоритовых, флюоритовых, графитовых, баритовых и других руд, а также полеошпатового сырья. Метод флотационного обогащения находит применение при обогащении железных и марганцевых руд. Широкая распространенность флотации объясняется универсальностью процесса, связанной с возможностью разделения практически любых минералов и возможностью обогащения бедных руд.
Сущность процесса пенной флотации: исходная пульпа после обработки ее флотационными реагентами поступает во флотационную машину, где насыщается воздухом в виде мелких воздушных пузырьков. Гидрофобные частицы при столкновении с пузырьками прилипают к ним, создавая агрегаты, состоящие из воздушных пузырьков с закрепившимися на них твердыми частицами. Агрегаты, имеющие плотность меньшую плотности пульпы, всплывают на ее поверхность, образуя слой минерализованной пены, которая удаляется с поверхности. Гидрофильные частицы к воздушным пузырькам не прилипают, остаются в объеме пульпе и образуют камерный продукт.
Обычно в пенный продукт флотации извлекают полезный минерал, а в камерный – минералы пустой породы. Такой процесс носит название прямой флотации. В отдельных случаях целесообразнее в пенный продукт извлекать минералы пустой породы, полезные минералы концентрировать в камерном продукте. Такой процесс – обратная флотация.
Если в процессе флотации получают концентрат, содержащий два или более ценных компонентов (ЦК), такую флотацию называют коллективной.
Если в процессе флотации последовательно получают несколько концентратов при содержании в каждом отдельном только одного ЦК, то это селективная флотация.
Если в процессе флотации вначале получают коллективный концентрат, а затем из него выделяют последовательно ЦК в самостоятельные концентраты, то это коллективно-селективная флотация.
Т.к. в один прием не всегда удается получить концентрат с достаточным содержанием полезного компонента (ПК) и бедные по содержанию ПК отходы, операции обогащения повторяются. Операции дообогащения чернового концентрата называются перечистными, а операции, связанные с доизвлечением ПК из хвостов, называются контрольными.
| Изм.руда |
| Контрольная флотация |
| Основная флотация |
| I перечистка |
| II перечистка |
| 50% кл.-0,074мм |
| п.п. |
| к.п. |
| хвосты |
| п.п. |
| к.п. |
| п.п. |
| концентрат |
| к.п. |
ОПРЕДЕЛЕНИЯ, ПОНЯТИЯ ФЛОТАЦИОННОГО ПРОЦЕССА
Флотация – это в общем виде «плавание» или «всплывание».
Основываясь на внешних признаках, процесс флотации можно было бы определить как способ разделения минералов, при котором одни минералы всплывают на поверхность пульпы, а другие тонут. Однако такое определение было бы недостаточным. Во-первых, оно исходит только из внешней стороны процесса и не отражает существа явлений, происходящих при флотации. Во-вторых, в настоящее время известны такие флотационные процессы, при которых никакого всплывания или плавания частиц нет. Между тем эти процессы обусловлены теми же причинами, что и обычная флотация.
Для правильного определения понятия «флотационный процесс обогащения» следует рассмотреть существо процесса и установить основные причины, вызывающие его.
Процесс флотации основан на II законе термодинамики, который имеет множество формулировок, связанных между собой. И если справедлива одна из формулировок, то и справедливость основных может быть доказана.
При рассмотрении физико-химических процессов наиболее удобнее следующие формулировки этого закона:
1. Во всякой системе при постоянных температуре и объеме самопроизвольно могут протекать лишь те процессы, которые сопровождаются уменьшением ее свободной энергии;
2. Всякая система при постоянных температуре и объеме стремится перейти в такое состояние, при котором ее свободная энергия будет наименьшей.
Свободная энергия системы равна максимальной работе, которую она может совершить при постоянных температуре и объеме.
В первой формулировке говорится, что процессы могут протекать самопроизвольно, но не утверждается, что они будут протекать в действительности.
Во второй формулировке сказано, что система может самопроизвольно перейти в состояние, но не утверждается, что она обязательно перейдет в него.
Поэтому приведенные формулировки следует уточнить: всякая система при постоянных температуре и объеме самопроизвольно перейдет из состояния, в котором она обладает более высокой свободной энергией, в состояние, соответствующее более низкой свободной энергии, если на пути перехода нет энергетических барьеров, или если системе будет сообщена энергия, достаточная для преодоления этих барьеров. Эта энергия называется энергией активации.
Для установления причин и сущности флотационного процесса рассмотрим возможные положения частиц малых размеров кубической формы относительно границы раздела двух фаз (например: масла и воды).
| м |
| в |
| а |
| а |
Фаза – часть гетерогенной (разнородной) системы, отделенная от других частей видимой границей раздела и обладающая одинаковыми химическими и термодинамическими свойствами. К термодинамическим относят такие свойства вещества, которые изменяются при изменении температуры и давления.
Чтобы решить вопрос о том, в каком из четырех положений будет находиться частица, надо определить свободную энергию системы для каждого из этих положений.
В соответствии со вторым законом термодинамики частица займет положение, при котором свободная энергия будет наименьшей. Свободная энергия рассматриваемой системы будет складываться из ее потенциальной энергии, зависящей от высоты центра тяжести частицы, и поверхностной энергии системы, также зависящей от положения частицы. Поверхностная энергия какой-либо поверхности раздела фаз определяется произведением площади этой поверхности на удельную поверхностную энергию. Потенциальная энергия частицы пропорциональна ее весу или объему, т.е. пропорциональна d3 (длина ребра куба). Поверхностная энергия частицы пропорциональна ее поверхности, т.е. d2. При уменьшении размера частицы величина ее потенциальной энергии будет падать быстрее, чем величина поверхностной энергии. Например, при уменьшении диаметра частицы в 10 раз потенциальная энергия уменьшится в 1000 раз, а поверхностная – в 100 раз. Поэтому, какой бы малой ни была поверхностная энергия по сравнению с потенциальной, можно всегда взять частицу столь малых размеров, для которых поверхностная энергия будет намного больше потенциальной. В этом случае потенциальной энергией можно пренебречь. Для частиц больших размеров потенциальная энергия будет больше поверхностной, и направление процесса будет определяться изменением потенциальной энергии.
Рассмотрим случай, когда частица имеет столь малые размеры, что ее потенциальная энергия очень мала по сравнению с поверхностной. При этом условии изменение потенциальной энергии системы будет незначительно по сравнению с изменением поверхностной энергии.
Для записи уравнений поверхностной энергии в первых четырех положениях применимы следующие обозначения:
d – размер ребра частицы;
σ1-2 – удельная поверхностная энергия на границе раздела 1-2;
σ1-т – удельная поверхностная энергия на границе раздела первой фазы и твердой частицы;
σ2-т – удельная поверхностная энергия на границе раздела второй фазы и твердой частицы;
Е – поверхностная энергия.




После вычитания из правых и левых частей равенства величины 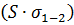 и деления на d2 получим следующие равенства:
и деления на d2 получим следующие равенства:




Т.к. в этих равенствах из значений Е1-Е4 вычитается постоянная величина 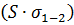 , и полученные разности делятся на d2, то наименьшее значение Е будет соответствовать наименьшему значению левой, а значит и правой части этих равенств. Но величина правых частей равенств определяется только значениями удельных поверхностных энергий на границах соприкасающихся фаз. Таким образом, рассмотрение вопроса о свободной поверхностной энергии приводит к выводу, что максимальное значение свободной энергии рассматриваемой системы при различных положениях частиц малых размеров определяется только величиной удельных поверхностных энергий на границе соприкасающихся фаз.
, и полученные разности делятся на d2, то наименьшее значение Е будет соответствовать наименьшему значению левой, а значит и правой части этих равенств. Но величина правых частей равенств определяется только значениями удельных поверхностных энергий на границах соприкасающихся фаз. Таким образом, рассмотрение вопроса о свободной поверхностной энергии приводит к выводу, что максимальное значение свободной энергии рассматриваемой системы при различных положениях частиц малых размеров определяется только величиной удельных поверхностных энергий на границе соприкасающихся фаз.
Согласно второму закону термодинамики, система придет в состояние, соответствующее минимальной свободной энергии. Поэтому положение, которое займет частица малых размеров по отношению к положению соприкосновения двух фаз, определяется только значениями удельных поверхностных энергий соприкасающихся фаз.
Если для двух частиц различного минералогического состава окажется, что минимальная свободная энергия системы для одной частицы будет соответствовать одному из первых трех ее положений, а для второй – четвертому положению, то такие частицы могут быть разделены, т.к. после их соприкосновения с межфазовой поверхностью первая частица будет оставаться у поверхности раздела фаз, а вторая перейдет в нижнюю фазу и будет находиться внутри. Такой способ разделения называется флотационным.
Флотационные процессы – процессы разделения минералов, основанные на различительной способности этих минералов закрепляться на межфазовой поверхности, которая определяется границей в удельных поверхностных энергиях разделяемых минералов на границах с жидкой и газообразными фазами.
Если минимальное значение поверхностной энергии системы будет соответствовать одному из первых трех положений частицы, то частица называется флотирующейся. Если положению IV, то нефлотирующейся.
Таким образом, флотация основана на различиях в свойствах разделяемых минералов, т.е. на различиях в удельных поверхностях на границе раздела соприкасающихся фаз.
ЭЛЕМЕНТАРНЫЙ АКТ ФЛОТАЦИИ.
ГИПОТЕЗА КРАЕВОГО УГЛА.
| воздух |
| вода |
| стекло |
| А1 |
| А2 |
Явление смачиваемости наблюдается при соприкосновении трех фаз. Две соприкасающиеся фазы образуют межфазовую поверхность. При пересечении этой поверхности с поверхностью третьей фазы образуется линия соприкосновения трех фаз, которая называется периметром смачивания (А1-А2). Краевым углом смачивания называется угол, образованный поверхностью раздела двух фаз с поверхностью третьей фазы.
Если при образовании краевого угла отсутствует гистерезис, то угол называется равновесным; в противном случае образуется гистерезисный краевой угол. Равновесный краевой угол является физико-химической константой для данных трех фаз, определяемой величиной удельных поверхностных энергий на поверхности раздела этих фаз.
Силы, действующие на единицу длины периметра смачивания, не находятся в равновесии, т.к. сила, направленная вверх, больше силы, направленной вниз. Вследствие этого периметр смачивания будет перемещаться вверх, при этом краевой угол будет уменьшаться. Вследствие чего появляется вертикальная составляющая силы, направленная вниз (по мере уменьшения краевого угла она возрастает). При некотором значении краевого угла силы, действующие на единицу длины периметра смачивания вверх и вниз, станут равными, т.е. наступит равновесие сил.
Угол, отвечающий равновесию сил поверхностного натяжения, называется равновесным краевым углом.
Условная классификация гидрофильности и гидрофобности:
1. Тело абсолютно гидрофильно, если вода распространяется по всей его поверхности;
2. Тело частично гидрофильно, если вода частично вытесняет воздух с поверхности тела; при этом равновесный краевой угол будет острым;
3. Тело частично гидрофобно, если воздух частично вытесняет воду с поверхности тела; при этом равновесный краевой угол – тупой;
4. Тело абсолютно гидрофобно, если воздух распространяется по всей поверхности тела, вытесняя воду.
ПОКАЗАТЕЛЬ ФЛОТИРУЕМОСТИ
| Г |
| Т |
| Ж |
| Ж |
| Г |
| Т |
Если свободная энергия системы во втором состоянии меньше, чем в первом, то система из первого состояния самопроизвольно перейдет во второе при условии, что на пути перехода нет энергетического барьера или если системе временно сообщена энергия для преодоления барьера (энергия активации). Чем больше разница в величине свободной энергии, тем более вероятен переход в состояние с меньшей энергией.
Свободная поверхностная энергия в первом состоянии:

Во втором состоянии: 
Изменение поверхностной энергии: 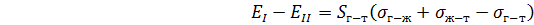
Разница поверхностных энергий, относящаяся к единице площади:

F – показатель флотируемости
Если F>0, то EI>EII, и система из первого состояния перейдет во второе, т.е. при соприкосновении частицы с поверхностью раздела Г-Ж должно произойти ее закрепление.
Если F<0, то закрепление невозможно.
Таким образом, чем больше значение F, тем вероятнее закрепление и реализация процесса флотации.
Показатель флотируемости – изменение поверхностной энергии системы при элементарном акте флотации, отнесенное к единице площади контакта Г-Т.
Связь между краевым углом и показателем флотируемости:
Показатель флотируемости и краевой угол зависят от удельных поверхностных энергий на границах соприкасающихся фаз:
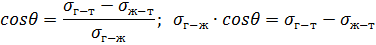

Следовательно, чем больше краевой угол, тем выше показатель флотируемости.
ПОНЯТИЕ О ГИДРАТНЫХ СЛОЯХ
В тонком пограничном слое, примыкающем к поверхностям раздела фаз, молекулы находятся в особом энергетическом состоянии, отличном от состояния молекул, расположенных в остальном объеме фазы, из-за неуравновешенности сил, действующих на молекулы пограничного слоя со стороны соприкасающихся фаз. Вследствие этого свойства жидкости, находящиеся в пограничном слое, отличаются от свойств жидкости, находящейся в объеме. Если в качестве жидкости взята вода, то ее пограничные слои называются гидратными слоями. Они образуются как у границы раздела «вода-твердое», так и с газообразной и жидкой фазами.
Если вода соприкасается с очень полярной фазой, то под действием электростатических сил диполи воды пограничного слоя будут строго ориентированы. Ориентировка молекул пограничного слоя вызывает ориентировку, однако, уже ослабленную, у молекул более глубоких слоев. По мере удаления от твердой поверхности под действием молекулярного движения ориентировка все более нарушается, и гидратный слой постепенно переходит в обычную воду. Толщина гидратных слоев может достигать нескольких сотых долей микрона. Если толщина гидратного слоя между взаимодействующими фазами большая, и они не соприкасаются, то удельная поверхностная энергия прослоя будет оставаться постоянной и равной сумме поверхностных энергий на границе «Ж-Г» и «Ж-Т». Как только происходит соприкосновение гидратных слоев, свойства промежуточного прослоя воды будут непрерывно изменяться, что вызовет изменение удельной поверхностной энергии прослоя. Для закрепления на поверхности «Ж-Г» частица должна преодолеть энергетический барьер. Этот барьер преодолевается за счет кинетической энергии частицы. После закрепления частицы между твердой и газообразной фазами остается устойчивый гидратный слой, свойства которого должны отличаться от свойств обычной воды. И т.к. после закрепления частицы между твердой и газообразной фазами остается остаточный гидратный слой, то удельную поверхностную энергию на границе раздела «Г-Т» можно рассматривать как сумму двух поверхностных энергий.
ФЛОТАЦИОННЫЕ РЕАГЕНТЫ.
НАЗНАЧЕНИЕ И КЛАССИФИКАЦИЯ
Чем больше показатель флотируемости, тем вероятнее закрепление минералов на пузырьках воздуха. Увеличение числа пузырьков в пульпе повышает вероятность столкновения с ним минеральных частиц. При одном и том же количестве подаваемого во флотационную машину (ФМ) воздуха уменьшение размера пузырьков приводит к увеличению их числа, а, следовательно, и повышению скорости флотации. При неустойчивой пене пузырьки при выходе на поверхность быстро лопаются, и прикрепившиеся к ним частицы минерала снова погружаются в пульпу. Это вызывает снижение извлечения минералов в концентрат. Изменение показателей флотируемости раздельных минералов, числа и размера пузырьков воздуха и прочности пены достигается применением флотационных реагентов.
В зависимости от места действия реагенты делятся на 2 класса:
1. Реагенты, непосредственно взаимодействующие или регулирующие взаимодействие других реагентов с поверхностью минерала, т.е. реагент, действующие на границе «Ж-Т».
2. Реагенты, действующие на поверхности раздела «Г-Ж».
Реагенты первого класса делятся на 4 группы:
1. Коллекторы или собиратели – органические вещества, способные закрепляться на поверхности отдельных минералов и увеличивать их флотируемость.
2. Депрессоры или подавители – реагенты, понижающие флотируемость тех минералов, извлечение которых в пенный продукт нежелательно; они препятствуют закреплению собирателя на поверхности минерала.
3. Активаторы или побудители – реагенты, способствующие закреплению собирателя на поверхности минералов. Их действие противоположно действию депрессоров.
4. Регуляторы среды – реагенты, влияющие на процесс взаимодействия других групп реагентов с минералами. Они регулируют ионный состав пульпы, процесс диспергирования и коагуляции тонких частиц шламов.
Депрессоры, активаторы и регуляторы среды относят к одной группе и называют модификаторами.
Реагенты второго класса – пенообразователи или вспениватели.
Вспениватели облегчают диспергирование воздуха на мелкие пузырьки, препятствуют их слиянию (коалесценции) и повышают прочность пены.
Ко всем флотореагентам предъявляются следующие требования: селективность действия, стандартные качества, дешевизна и недефицитность, удобство в применении, легкая растворимость в воде, отсутствие неприятного запаха, нетоксичность и т.д.
ДВОЙНОЙ ЭЛЕКТРИЧЕСКИЙ СЛОЙ
Вследствие взаимодействия минералов с водой и присутствующими в ней ионами на разделе «Ж-Т» возникает двойной электрический слой. Энергия взаимодействия молекул воды с различными ионами минерала неодинакова. Ионы различных знаков переходят в раствор в неэквивалентных количествах, и поверхность минерала получает заряд. Знак заряда совпадает со знаком ионов минерала, переходящих в раствор в меньшем количестве. Заряд на поверхности минерала может возникать и результате преимущественной адсорбции из раствора ионов одного знака. К заряженной поверхности из раствора притягиваются ионы противоположного знака. Образуется двойной электрический слой. Увеличение заряда поверхности затрудняет дальнейший переход ионов противоположного знака в раствор, поэтому при некотором значении заряда устанавливается равновесие.
Поверхность галенита, помещенного в дистиллированную воду:
| A |
| PbS |
| K |
| A |
| К2 |
| К2 |
| K |
Поверхность галенита, помещенного в воду, получит отрицательный заряд за счет преимущественного перехода в раствор ионов свинца (Pb+2). После того, как установится равновесие между раствором и твердой фазой, левее первой плоскости будет неизменяемая кристаллическая решетка галенита, а правее анионов будет больше, чем катионов. Вторая плоскость – физическая граница минерала. Анионы кристаллической решетки, расположенные между первой и второй плоскостями, образуют внутреннюю обкладку двойного электрического слоя (А). около поверхности минерала (за второй плоскостью) располагаются противоионы, перешедшие в раствор. Они составляют внешнюю обкладку двойного электрического слоя. Противоионы, прилегающие ко второй плоскости, прочно связаны с заряженной поверхностью минерала и находятся в упорядоченном состоянии. При движении минералов в жидкости они перемещаются вместе с минералами. Противоионы, расположенные в слое К, - упорядоченная часть внешней обкладки двойного электрич.слоя или слой Штерна. Противоионы правее третьей плоскости слабо связаны с поверхностью минерала. Вследствие молекулярного движения их расположение неупорядоченно, а концентрация по мере удаления от поверхности минерала постепенно убывает. При относительном перемещении минерала и жидкости они отстают от минерала. Это диффузионный слой или слой Гюи. Т.к. поверхность частицы имеет заряд, то в пространстве, окружающем частицу, появляется электрическое поле. Потенциал любой точки поля определяется работой, затрачиваемой или получаемой при переносе единицы электричества из бесконечно удаленной точки в данную точку поля. Потенциал на поверхности частицы называется полным или термодинамическим. А потенциал на границе третьей поверхности – электрокинетическим или дзета-потенциалом. Заряд поверхности, термодинамический и электрокинетический потенциалы играют большую роль при взаимодействии реагента с минералами. Поверхности частиц, имеющие большой заряд, притягивают диполи воды и ориентируют их в пограничном слое. Вода образует на границе с такой поверхностью прочный гидратный слой и хорошо смачивает минерал. Вытесняются диполи воды ионами реагента, если реагент более прочно связывается с минералом, чем диполи воды. Отрицательный заряд поверхности затрудняет физическую адсорбцию минералов анионов и облегчает адсорбцию катионов. Положительный заряд оказывает противоположное действие. При хемосорбции или гетерогенной химической реакции заряд поверхности может не оказать заметного влияния, т.к. химические силы связаны прочнее электростатических. Величина термодинамического потенциала изменяется при изменении в растворе концентрации потенциала определяющих ионов. А величина дзета-потенциала – при изменении концентрации любых электролитов в растворе.
КОЛЛЕКТОРЫ ИЛИ СОБИРАТЕЛИ.
СУЛЬФГИДРИЛЬНЫЕ СОБИРАТЕЛИ
К этому классу реагентов относятся органические производные угольной кислоты, которые называются ксантогенатами. От угольной кислоты получаются производные, которые называются дитиоугольными кислотами. Их образование происходит путем замещения атомов водорода атомами серы. При замене в тиоугольных кислотах атома водорода углеводородным радикалом получают алкилтиоугольные кислоты.
Соли щелочных металлов этих кислот алкилтиокарбонаты устойчивые и хорошо растворимы в воде. Они обладают собирательной способностью по отношению к сульфидам тяжелых металлов и по отношению к самородным металлам. Активность собирателей возрастает с увеличением длины углеводородной цепи и зависит от числа атомов серы в молекуле. Поэтому алкилмонотиокарбонаты слабые собиратели, а алкилтритиокарбонаты – сильные.
Ксантогенаты щелочных металлов более растворимы, чем щелочно-земельных, а тяжелых металлов – мало растворимы. Флотируемость сульфидов и самородных металлов ксантогенатами зависит от растворимости соответствующих ксантогенатов тяжелых металлов. Лучше флотируются сульфиды, с металлами которых ксантогенатный ион образует менее растворимые соли. С увеличением длины углеводородной цепи уменьшается растворимость ксантогенатов, а их флотационная активность и гидрофобизирующее действие при одинаковой плотности адсорбируемого слоя возрастает.
В практике обогащения сульфидных руд наибольшее применение получил бутиловый ксантогенат. Ксантогенаты могут окисляться и переходить в диксантогениды (маслянистая мало растворимая в воде жидкость, флотирует сульфиды также хорошо, как и ксантогенаты). При взаимодействии с сульфидами диксантогениды восстанавливаются до ксантогенатов. Присутствие в пульпе некоторого количества диксантогенида полезно, т.к. он закрепляется на участках поверхности минералов, покрытых ксантогенатом. Повышает гидрофобность этих участков и облегчает закрепление частиц на пузырьках.
Следующий класс сульфидных собирателей называется дитиокарбонатами. Они получаются при замене в угольной кислоте гидроксильной группы на аминогруппу. Эти кислоты нестойкие, но дают соли и эфиры, которые более устойчивые. Заменив в группе NH2 атомов водорода углеводородными радикалами , получается диэтилдитиокарбонат натрия, который является сильным собирателем для сульфидов.
Органические производные дитиофосфорной кислоты также относятся к классу сульфидных собирателей. Их можно рассматривать как фосфорную кислоту, в которой атомы кислорода замещены атомами серы, а атомы водорода углеводородными радикалами.
Жидкие аэрофлоты – дитиофосфорные кислоты. Соли щелочных металлов этих кислот называют твердыми или сухими аэрофлотами. Как собиратели аэрофлоты слабее ксантогенатов, но более устойчивы в кислых средах и не окисляются кислородом воздуха, содержащимся в пульпе. Жидкие аэрофлоты содержат некоторое количество непрореагированного крезола, поэтому они обладают еще и пенообразующими саойствами.
В России наиболее широко применяется бутиловый аэрофлот – дибутилдитиофосфат натрия. Получается он при взаимодействии бутилового спирта и пятисернистого фосфора с последней нейтрализацией дибутилдитиофосфатной кислоты щелочью. Бутиловый аэрофлот хорошо растворим в воде, флотирует сульфиды, пенообразующими свойствами не обладает, собирательные свойства его слабее, чем у ксантогенатов.
Обычно в технологиях флотации сульфидных руд ксантогенаты и аэрофлоты применяются одновременно.
ОКСИГИДРИЛЬНЫЕ СОБИРАТЕЛИ
Это органические производные угольной кислоты.
При взаимодействии высокомолекулярных карбоновых кислот со щелочами образуются соединения, называемые мылами. Высокомолекулярные карбоновые кислоты, называемые жирными, и их мыла щелочных металлов являются собирателями, которыми можно флотиравать почти все минералы.
Собирательная способность жирных кислот зависит от строения углеводородной цепи и наличия в ней двух связей.
При небольшом числе атомов углерода в аполярной группе молекулы разветвление цепи приводит к понижению собирательных свойств реагента. А при значительном – к повышению. Ненасыщенные жирные кислоты – более сильные собиратели, чем насыщенные при одинаковом числе атомов углерода в цепи. Из карбоновых кислот наиболее изучена как собиратель алеиновая кислота. Она является не насыщенной кислотой и имеет одну двойную связь посередине углеводородной цепи. Соответствующая ей насыщенная жирная кислота – стеориновая.
Эти кислоты являются главными составными частями животных и растительных жиров. Соли этих кислот со щелочами металлов называются твердыми и жидкими мылами. Жирные кислоты – хорошие собиратели для не содержащих кремнозем солей щелочно-земельных металлов и карбонатов черных металлов. Ими хорошо флотируются: кальцит, флюорит, шеелит, апатит, барит, сидерит. Несколько хуже флотируются окислы: бурые железняки, гематит, магнетит. Силикаты флотируются жирными кислотами, если они не содержат металлы, способные образовать с жирной кислотой трудно растворимые поверхностные соединения. Чистый кварц жирными кислотами не флотируется.
1. Влияние температуры. Алеиновая кислота – жидкость, замерзающая при температуре +140С. Поэтому при низких температурах она переходит в твердую фазу, и ее флотационная активность резко падает. Для повышения активности жирных кислот при низких температурах применяют органические растворители (керосин, ОП-4, эмульгаторы) или подогревают пульпу.
2. Влияние рН. Все карбоновые кислоты, в том числе и алеиновая, - слабые кислоты. Поэтому при гидролизе их солей образуются жирные кислоты и щелочи. Гидролиз тем сильнее, чем меньше щелочность пульпы. Высшие жирные кислоты обладают малой растворимостью. Поэтому производные активностей являются величиной постоянной. Только в щелочных пульпах можно получить высшую концентрацию алеиновой кислоты, а в кислых пульпах основное количество реагентов находится в нерастворимом виде, образуя эмульсию. Активность и собирательные свойства алеиновой и других жирных кислот, их мыл в сильной степени завися от рН пульпы – собирательная способность возрастает с увеличением рН. Гидроксильные ионы при высокой концентрации сильно депрессируют некоторые минералы. Для таких минералов флотационная активность карбоновых кислот и их мыл будет выше в слабощелочной и слабокислой средах.
3. Влияние жесткости воды. Собирательные свойства жирных кислот зависят от жесткости воды, которая определяется концентрацией ионов магния и кальция. Они образуют с высшими карбоновыми кислотами трудно растворимые мыла. Что приводит к потере собирателя и нарушению селективности процесса. Поэтому карбоновые кислоты не эффективны в жесткой воде.
Алеиновая кислота и ее мыло мало селективные собиратели. Селективность их действия можно повысить подбором оптимальных дозировок реагентов – модификаторов, например, соды и жидкого стекла. При флотации сильно шламующихся минералов расход собирателя увеличивается.
Заменители алеиновой кислоты:
1. Сульфатное мыло является побочным продуктом целлюлозного производства. Содержит до 60% натриевых солей жирных и аполярных кислот. Служит исходным продуктом для получения талового масла. При флотации используется редко.
2. Таловое масло. Сырое таловое масло получается разложением сульфидного мыла серной кислотой. Активные компоненты этого собирателя – жирные и смоляные кислоты. Таловые масла при употреблении обычно омыляются щелочами.
3. Нафтеновые кислоты – карбоновые кислоты, у которых радикал представлен остатками нафтенов – это углеводороды с замкнутой цепью, соединяющие 5 или 6 метеленовых групп. Нафтеновые кислоты содержатся в небольших количествах в нефти. При обработке нефти раствором щелочи они переходят в водную фазу в виде растворимых мыл. После отделения от нефти водная фаза подвергается обработке серной кислотой. При этом опять образуются нафтеновые кислоты. Нафтеновые кислоты и мыло-нафты обладают более слабыми собирательными свойствами, чем алеиновая кислота и таловое масло, и более сильным пенообразующим действием.
КАТИОННЫЕ СОБИРАТЕЛИ
К ним относятся органические ПАВ, у которых при диссоциации гидрофобный радикал переходит в положительно заряженный ион-катион. Основные активные собиратели: жирные амины и их соляно-кислые и уксусные соли.
Амины можно рассматривать как производные аммиака. Они обладают свойствами слабых оснований, основное свойство которых: реакция идет в двух направлениях. Степень их диссоциации зависит от рН среды и возрастает с повышением ионизации водородных анионов. Амины, в радикале которых содержится более 6 атомов Н, в воде практически нерастворимы, поэтому при флотации используют их соли. Полученные соляной или уксусной кислотой.
Типы катионных собирателей:
1. Катионный реагент АНП (амины из нитропарафинов).
АНП получают путем каталитического восстановления нитропарафинов, полученных обработкой углеводородной фракции С11-С16 азотной кислотой.
Реагенты АНП – смесь хлоргидратов первичных атомов, содержащих 14 атомов углерода.
2. Амины на основе высших жирных кислот.
При гидрирующем аминировании высших жирных кислот нормального строения получаются жирные амины нормального строения.
На основе жирных кислот животного происхождения производятся октодециламин и амины на основе фракций С17-С20.
АПОЛЯРНЫЕ СОБИРАТЕЛИ
Они не содержат в своей структуре полярных групп, поэтому практически не взаимодействуют с водой и поверхностью полярных минералов. Обладают способностью селективно закрепляться на поверхности гидрофобизированных минералов. Основные аполярные собиратели: углеводороды (углеводородны
Последнее изменение этой страницы: 2016-06-09
lectmania.ru. Все права принадлежат авторам данных материалов. В случае нарушения авторского права напишите нам сюда...