
Категории:
ДомЗдоровьеЗоологияИнформатикаИскусствоИскусствоКомпьютерыКулинарияМаркетингМатематикаМедицинаМенеджментОбразованиеПедагогикаПитомцыПрограммированиеПроизводствоПромышленностьПсихологияРазноеРелигияСоциологияСпортСтатистикаТранспортФизикаФилософияФинансыХимияХоббиЭкологияЭкономикаЭлектроника
КЛАССИФИКАЦИЯ И НОМЕНКЛАТУРА ФЕРМЕНТОВ
Катализируемая химическая реакция представляет собой тот специфический признак, по которому один фермент отличается от другого. Поэтому естественно и логично, что классификация и номенклатура ферментов основывается на этом принципе. Современная классификация ферментов разработана специальной Комиссией Международного Биохимического Союза и изложена в книге "Номенклатура ферментов", которая вышла в русском переводе в 1979 г.
В основе классификации лежат три положения:
а) все ферменты делятся на 6 классов по типу катализируемой реакции;
б) каждый фермент получает систематическое название, включающее название субстрата, тип катализируемой реакции, и окончание "аза"; кроме того, Комиссией были сохранены и узаконены тривиальные названия. Таким образом, возникла двойная система наименования ферментов;
в) каждому ферменту присваивается четырехзначный шифр (код). Первое число указывает класс ферментов, второе — подкласс, третье — подподкласс, четвертое — порядковый номер фермента в подподклассе.
Например, алкогольдегидрогеназа (Н.Ф.1.1.1.1): первая цифра — 1 — означает класс оксидоредуктаз, вторая цифра — 1 — подкласс дегидрогеназ (действует на СН — ОН-группу доноров), третья цифра — 1 — подподкласс анаэробные дегидрогеназы (акцептором служит НАД+ или НАДФ+), четвертая цифра — 1 — конкретный фермент алкогольдегидрогеназа.
Или α-амилаза (Н.Ф.3.2.1.1): первая цифра — 3 — класс гидролаз, вторая цифра — 2 — подкласс карбогидраз, третья цифра — 1 — подподкласс полиаз, четвертая цифра — 1 — конкретный фермент α-амилаза.
Современная международная классификация ферментов делит все ферменты на 6 основных классов:
1 класс — оксидоредуктазы — ферменты, катализирующие окислительно-восстановительные реакции (присоединение О2, отнятие и перенос Н2, перенос электронов);
2 класс — трансферазы — ферменты переноса. Катализируют перенос целых атомных группировок с одного соединения на другое (например, остатков моносахаридов, аминокислот, остатков фосфорной кислоты, метальных и аминных групп и т.д.);
3 класс — гидролазы — ферменты, катализирующие реакции гидролиза, то есть расщепления сложных органических соединений на более простые с участием воды. Эти реакции могут быть выражены следующим уравнением: RR1 + НОН → R — OH + R1 — H;
4 класс — лиазы — ферменты, катализирующие реакции негидролитического отщепления каких-либо групп от субстрата с образованием двойной связи или присоединение группировок по месту разрыва двойной связи (например, отщепление Н2О, СО2, NH3 и т.д.);
5 класс — изомеразы — ферменты, катализирующие реакции изомеризации, то есть внутримолекулярного переноса химических группировок и образование изомерных форм различных органических соединений;
6 класс — лигазы (синтетазы) — ферменты, катализирующие реакции синтеза, сопряженные с разрывом высокоэнергетической связи АТФ и других нуклеозидтрифосфатов (при этом возможно образование С-С-; C-S-; С-О-; и C-N- связей).
В табл. 8.2 представлены шифры, принятые для различных ферментов, их систематические и тривиальные названия. В таблицу включены лишь ферменты, имеющие принципиальное значение при хранении, переработке сырья и в производстве пищевых продуктов. В дальнейшем, везде где это возможно, будут применяться тривиальные названия.
Внимание технологов, перерабатывающих биологическое сырье, привлекают прежде всего ферменты 1-го класса — оксидоредуктазы, а также 3-го класса — гидролазы, поскольку при переработке пищевого сырья происходит разрушение клеточной структуры биологического материала, повышается доступ кислорода воздуха к измельченным тканям и создаются благоприятные условия для действия ферментов типа оксигеназ, а также высвобождаются гидролитические ферменты, которые активно расщепляют все основные структурные компоненты клетки (белки, липиды, полисахариды), в связи с чем процессы распада клеточного содержимого (процессы автолиза, самопереваривания) становятся преобладающими.
Таблица. 8.2.Номенклатура ферментов, имеющих значение в пищевой промышленности ["Номенклатура ферментов", Рекомендации 1972 г. — М., 1979 (под ред. акад. А. Е Браунштейна)]
| Шифр | Систематическое название | Тривиальное название |
| Оксидоредуктазы | ||
| 1.1.3.4 | β-D-глюкоза: О2-оксидоредуктаза | Глюкозооксидаза |
| 1.11.1.6 | Н2О2: Н2О2-оксидоредуктаза | Катал аза |
| 1.14.18.1 | Монофенол, дигидрооксифенилаланин: О2-оксидоредуктаза | Монофенолоксидаза, полифенолоксидаза, тирозиназа, фенолаза |
| Гидролазы | ||
| 3.1.1.3 | Триацилглицерол — ацилгидролаза | Липаза, триацилглицероллипаза |
| 3.1.1.11 | Пектин-пектилгидролаза | Пектинэстераза |
| 3.2.1.1 | 1,4-α-О-глюкан глюканогидролаза | α-Амилаза |
| 3.2.1.2 | 1,4-α-О-глюкан мальтогидролаза | β-Амилаза |
| 3.2.1.3 | 1 ,4-α-О-глюкан глюкогидролаза | γ-Амилаза, глюкоамилаза |
| 3.2.1.4 | 1 ,4-β-О-глюкан-4-глюкангидролаза | Целлюлаза |
| 3.2.1.15 | Поли-α- 1 ,4-галактуронид-гликаногидролаза | Полигалактуроназа |
| 3.2.1.20 | α-D-глюкозид глюкогидролаза | α-Гликозидаза |
| 3.2.1.21 | D-глюкозид глюкогидролаза | β-Гликозидаза |
| 3.2.1.23 | β-D-глюкозид галактогидролаза | Лактаза, β-галактозидаза |
| 3.4.23.1 | — | Пепсин |
| 3.4.23.4 | — | Химозин (реннин) |
| 3.4.21.4 | — | Трипсин |
| 3.4.21.1 | — | Химотрипсин |
| 3.4.22.5 | — | Эластаза |
| 3.4.21.1 | — | Папаин |
| 3.4.21.6 | — | Химопапаин |
| 3.4.22.6 | — | Фицин |
| 3.4.22.3 | — | Бромелаин |
| 3.4.22.14 | — | Субтилизин |
| 3.4.23.6 | — | Кислая протеиназа |
| 3.4.24.3 | — | Коллагеназа |
| Изомеразы | ||
| 5.3.1.9 | D-глюкозо-6-фосфат-кетолизомераза | Глюкозоизомераза, глюкозофосфат-изомераза |
Остановимся на рассмотрении отдельных представителей этих двух важнейших для пищевой промышленности классов ферментов с позиции описания их свойств, активности, механизма реакции и коснемся вопросов практического применения, которые будут рассмотрены более подробно в разделах, посвященных применению ферментов в конкретных пищевых технологиях.
Оксидоредуктазы
Полифенолоксидаза(Н.Ф. 1.14.18.1). Этот фермент известен под различными тривиальными названиями: о-дифенолоксидаза, тирозиназа, фенолаза, катехолаза и др. Фермент может катализировать окисление моно-, ди-, и полифенолов.
Типичная реакция, катализируемая полифенолоксидазой, имеет вид:

Молекула фермента обладает четвертичной структурой и имеет молекулярную массу около 34 000 Да. Полифенолоксидаза — купропротеид. Содержание меди — 0,2%, или один атом Си на 1 молекулу фермента. Зона оптимальной активности лежит между рН 5,0 — 7,0.
В зависимости от того, из какого источника выделен фермент, способность его к окислению различных фенолов различна. Более того, даже в одном и том же объекте Полифенолоксидаза может содержаться в виде различных молекулярных форм, отличающихся по способности к окислению различных фенолов.
С действием этого фермента связано образование темноокрашенных соединений — меланинов при окислении кислородом воздуха аминокислоты — тирозина. Потемнение срезов картофеля, яблок, грибов, персиков и других растительных тканей в большей степени или полностью зависит от действия полифенолоксидазы. В пищевой промышленности основной интерес к этому ферменту сосредоточен на предотвращении рассмотренного нами ферментативного потемнения, которое имеет место при сушке плодов и овощей, а также при производстве макаронных изделий из муки с повышенной активностью полифенолоксидазы. Эта цель может быть достигнута путем тепловой инактивации фермента (бланшировка), добавлением ингибиторов (NaHSO3, SO2, NaCl) или связыванием субстрата посредством метилирования.
Положительная роль фермента проявляется при некоторых ферментативных процессах: например, при ферментации чая. Окисление дубильных веществ чая под действием полифенолоксидазы приводит к образованию темноокрашенных и ароматических соединений, которые определяют цвет и аромат черного чая.
Каталаза (Н.Ф. 1.11.1.6). Этот фермент катализирует разложение пероксида водорода в соответствии со следующей реакцией:

Таким образом, фермент окисляет одну молекулу перекиси водорода до кислорода с одновременным восстановлением другой молекулы перекиси водорода до Н2О.
Каталаза относится к группе гемопротеиновых ферментов. Содержит 0,009% железа в виде геминовой группировки или 4 атома на одну молекулу фермента. Молекулярная масса ферментов, выделенных из различных объектов (дрожжей, растительных и животных тканей, микроорганизмов), лежит в пределах от 225 000 до 250 000 Да. Они имеют существенные различия в оптимуме рН (от 2 до 9), в термо- и рН-стабильности. Фермент ингибируется цианидом (обратимо), фенолами (обратимо лишь в слабой форме), щелочью и мочевиной (необратимо). Функцией каталазы в живом организме является защита клетки от губительного действия перекиси водорода.
Хорошим источником для получения промышленных препаратов каталазы являются культуры микроорганизмов и печень крупного рогатого скота.
Каталаза находит свое применение в пищевой промышленности при удалении избытка Н2О2 при обработке молока в сыроделии, где последняя используется в качестве консерванта; а также совместно с глюкозооксидазой применяется для удаления кислорода и следов глюкозы.
Пероксидаза (Н.Ф. 1.11.1.7). Пероксидазы могут быть определены как ферменты, катализирующие следующую реакцию:

Пероксидаза — двухкомпонентный фермент, представляющий собой сочетание тема и гликопротеида. Показано, что углеводная часть придает белку большую специфичность; предполагают, что углеводы стабилизируют трехмерную структуру фермента.
В настоящее время выделено и охарактеризовано большое число множественных форм фермента и доказано существование изоферментов, то есть тех форм ферментов, которые обусловлены генетически. В связи с этим принято говорить о целой системе пероксидаз, работающих в любом живом организме. Интересным представляется факт широкой субстратной специфичности пероксидаз по отношению к донорам водорода (1 -и субстрат), ими могут служить фенолы, амины, другие органические соединения; и строгой специфичности по отношению к акцептору водорода (2-й субстрат) — перекиси водорода. Механизм реакции, предположительно, основан на образовании комплексов фермент — донор и двух одновалентных ступеней окисления, как это отражает следующая схема:
Пероксидаза + Н2О2 = Комплекс I
Комплекс I + АН2 = Комплекс II + АН
Комплекс II + АН = Пероксидаза + А
Изучению пероксидазы были посвящены классические работы Г. Теореля, Б. Чанса, А. Н. Баха, Р. Шода. Наиболее активная Пероксидаза выделена из корней хрена. Ее молекулярная масса равна примерно 40 000 Да, изоэлектрическая точка 7,2. Фермент содержит один атом железа на молекулу. Он достаточно устойчив в растворах при величинах рН от 4 до 12; его термостабильность значительно выше термостабильности каталазы. Оптимум рН для пероксидазы хрена равен 7; при рН от 6 до 8 сохраняется 70% его активности.
Липоксигеназа (Н.Ф.1.13.11.12). Этот фермент катализирует окисление полиненасыщенных высокомолекулярных жирных кислот (линолевой и линоленовой) кислородом воздуха с образованием высокотоксичных гидроперекисей. Ниже приведена реакция, катализируемая этим ферментом:
R ....... СН2-СН=СН-СН2-СН=СН-СН2 ....... СООН
↓ + О2
R ....... СН2-СН=СН-СН=СН-С(ООН)Н-СН2 ....... СООН
Возможно образование и циклических гидроперекисей по следующей схеме:

Однако основное количество жирных кислот превращаются в гидроперекиси, обладающие сильными окислительными свойствами, и именно на этом основано использование липоксигеназы в пищевой промышленности.
Липоксигеназа впервые была выделена из семян сои в 1928 г. Последующие исследования показали, что липоксигеназа широко распространена и в других растительных объектах: пшенице и других злаках, в семенах масличных и бобовых культур, в картофеле, баклажанах и т. д.
Тем не менее самым богатым источником фермента является мука соевых бобов. Липоксигеназа, полученная в кристаллическом состоянии из семян сои, имеет молекулярную массу 102 000 Да, изоэлектрическую точку 5,4. Оптимумы рН для ферментов, выделенных из различных объектов, сильно различаются. Оптимум температуры липоксигеназы находится между 20 и 30°С.
В зерне пшеницы активность липоксигеназы колеблется в значительных пределах и является сортовым признаком. Кроме того, активность липоксигеназы связана с показателем жизнеспособности зерна. Она закономерно снижается со снижением всхожести зерна и может быть биохимическим тестом жизнеспособности семян. Значительная часть липоксигеназы пшеницы прочно связана с клейковинными белками и освобождается при обработке клейковинного комплекса раствором восстановленного глутатиона.
Липоксигеназе принадлежит важная роль в процессах созревания пшеничной муки, связанных с улучшением ее хлебопекарных достоинств. Образующиеся под действием фермента продукты окисления жирных кислот способны вызывать сопряженное окисление ряда других компонентов муки (пигментов, SH-групп клейковинных белков, ферментов и др.). При этом происходит осветление муки, укрепление клейковины, снижение активности протеолитических ферментов и другие положительные изменения.
В разных странах разработаны и запатентованы способы улучшения качества хлеба, основанные на использовании препаратов липоксигеназы (главным образом, липоксигеназы соевой муки). Все они требуют очень точного дозирования фермента, так как даже небольшая передозировка приводит к резко отрицательному эффекту и вместо улучшения качества хлеба происходит его ухудшение.
Более мягкий способ воздействия на компоненты муки и теста связан с активацией собственной липоксигеназы муки путем некоторого варьирования технологического процесса. При этом исключается эффект передозировки фермента со всем комплексом нежелательных последствий.
Использование липоксигеназы как улучшителя окислительного действия требует определенной осторожности, так как хорошо известна токсичность переокисленных жиров. Интенсивное окисление липоксигеназой свободных жирных кислот может сопровождаться вторичными процессами образования веществ различной химической природы с неприятным вкусом и запахом, характерным для прогорклого продукта. Технологически приемлема ограниченная степень окисления полиненасыщенных жирных кислот как промежуточного звена преобразования других компонентов биологического материала, не приводящая к накоплению фракции окисленных липидов.
Глюкозооксидаза (Н.Ф. 1.1.3.4). Этот фермент был впервые выделен еще в 1904 г. Н. А. Максимовым из плесневых грибов. Фермент представляет собой флавопротеид, в котором белок соединен с двумя молекулами ФАД. Он окисляет глюкозу с образованием в конечном счете глкжоновой кислоты и обладает практически абсолютной специфичностью по отношению к глюкозе. Суммарное уравнение имеет следующий вид:
Глюкоза + Н2О + О2 = глюконовая кислота + Н2О2
Представленный выше процесс на самом деле протекает в несколько стадий:
1-я стадия:
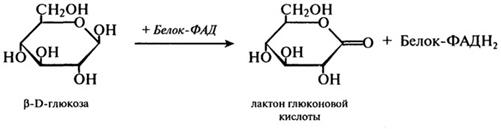
2-я стадия:

3-я стадия:
Белок-ФАД Н2 + О2 → Белок-ФАД + Н2О2
4-я стадия:

На первом этапе этой реакции происходит отнятие двух атомов водорода у первого углеродного атома глюкозы. При этом образуется восстановленный флавиновый фермент и лактон глюконовой кислоты. Далее восстановленный фермент реагирует с кислородом воздуха, и образуется перекись водорода. Токсичная перекись водорода расщепляется каталазой на кислород и воду, а β-О-глюконо-б-лактон подвергается спонтанному расщеплению с присоединением воды, в результате чего образуется глюконовая кислота.
Высокоочищенные препараты глюкозооксидазы получают из плесневых грибов рода Aspergillus и Penicillium. Они имеют примерно одинаковую молекулярную массу — около 150 000 Да, изоэлектрическую точку 4,2 — 4,3 и оптимум рН 5,6.
В последние годы глюкозооксидаза получила широкое применение. Благодаря исключительной специфичности препараты глюкозооксидазы применяются как аналитическое средство для количественного определения глюкозы.
Кроме этого, препараты глюкозооксидазы нашли применение в пищевой промышленности как для удаления следов глюкозы, так и для удаления следов кислорода. Первое — необходимо при обработке пищевых продуктов, качество и аромат которых ухудшаются из-за того, что в них содержатся восстанавливающие сахара; например, при получении из яиц сухого яичного порошка. Здесь имеется в виду реакция Майяра, т. к. глюкоза при сушке и хранении яичного порошка, особенно при повышенной температуре, легко вступает в реакцию с аминными группами аминокислот и белков. Порошок темнеет, и образуется ряд веществ с неприятным вкусом и запахом. Второе — необходимо при обработке продуктов, в которых длительное присутствие небольших количеств кислорода приводит к изменению аромата и цвета (пиво, вино, фруктовые соки, майонез). Внесение пакетиков, содержащих смесь воды, глюкозы, фермента и буфера, способствует удалению кислорода из воздушного пространства. Во всех подобных случаях в ферментную систему включают каталазу, разлагающую Н2О2, которая образуется при реакции глюкозы с кислородом. Этот метод нашел широкое применение в США для удаления кислорода из банок с сухим молочным порошком.
Гидролитические ферменты
Роль ферментов класса гидролаз в пищевых технологиях очень велика. Это находит отражение в специальной литературе, монографиях, технических инструкциях, стандартах. Поэтому в этом разделе остановимся на краткой характеристике наиболее важных представителей гидролитических ферментов. Для технологов наибольший интерес представляют три подкласса ферментов класса гидролаз. Это ферменты, действующие на сложноэфирные связи — эстеразы (Н.Ф.3.1); действующие на гликозидные соединения — гликозидазы (Н.Ф.3.2) и действующие на пептидные связи — протеазы (Н.Ф.3.4).
Эстеразы(Н.Ф.3.1). Этот подкласс включает большое число ферментов (около 150), которые разделены на семь подподклассов: ферменты, действующие на эфиры карбоновых кислот (3.1.1); эстеразы тиоловых эфиров (3.1.2); гидролазы фосфорных моноэфиров или фосфатазы (3.1.3); гидролазы фосфорных диэфиров (3.1.4); гидролазы моноэфиров олигофосфорных кислот (3.1.5); сульфатазы (3.1.6); эстеразы моноэфиров дифосфорных кислот (3.1.7).
Наиболее важными с точки зрения участия в различных биохимических процессах, имеющих место при хранении и переработке пищевого сырья, являются ферменты подподкласса 3.1.1.
Липаза (Н.Ф.3.1.1.3). Липаза или триацилглицероллипаза широко распространена в природе и играет важную роль в процессах, протекающих при переработке и хранении пищевых продуктов. В настоящее время выделены и охарактеризованы липазы растительного происхождения (липаза клещевины, пшеницы и других злаков), животного (панкреатическая липаза, липаза молока) и микробного (бактериальные и грибные липазы).
Обычно липазы катализируют реакцию расщепления триглицеридов согласно приведенному ниже суммарному уравнению:

Причем предпочтительнее гидролизуются связи в положении 3 и 1 и лишь затем в положении 2. Многочисленные экспериментальные данные дают основание предположить следующий путь липолиза:
триглицерид → 1,2-диглицерид → 2-моноглицерид → глицерин
Установлено, что липазы быстрее отщепляют остатки высокомолекулярных жирных кислот, чем низшие карбоновые кислоты. Ферментативный гидролиз липидов имеет существенное отличие от других гидролитических реакций. Парадокс заключается в том, что липаза — водорастворимый фермент, а ее субстрат гидрофобен; однако активность липазы возрастает на границе "вода — липид". Этот феномен известен под названием "межфазная активация".
Липазы различного происхождения сильно отличаются друг от друга по специфичности действия, сродству к различным субстратам, растворимости, оптимуму рН и другим свойствам. Так, например, липаза семян клещевины нерастворима в воде, имеет оптимум рН 4,7 — 5,0; панкреатическая липаза растворима, и оптимум рН ее действия лежит в слабощелочной среде. Липазы микробного происхождения и липаза пшеничных зародышей также отличаются от липазы клещевины. Они растворимы в воде и имеют рН оптимум при 8,0. Липаза молока, молекулярная масса которой примерно 7000 Да, имеет оптимум рН 9,0 — 9,2 при гидролизе молочного жира.
Зерновая липаза участвует в процессе порчи зерновых продуктов при хранении. Особенно это касается продуктов, содержащих повышенное количество жира, например, овсяной муки или крупы, пшена. Накопление свободных жирных кислот под действием липазы (рост кислотного числа жира) — признак ухудшения качества продукта. Свободные жирные кислоты, особенно ненасыщенные, легко подвергаются окислению под воздействием разных факторов: липоксигеназы, тепловой обработки, кислорода воздуха, солнечного света и др. Таким образом, липазы могут инициировать процесс прогоркания и ограничивать сроки хранения пищевых продуктов.
Одна из особенностей липаз связана с тем, что эти ферменты способны катализировать и обратную реакцию, осуществлять синтез сложных эфиров, а также производить переэтерефикацию триглицеридов, т. е. изменять их жирнокислотный состав. На этом основании разрабатываются способы получения новых форм жировых продуктов с использованием специфических липаз. Так, например, путем реакции переэтерифи-кации делаются попытки получения жира — аналога масла какао из дешевого исходного сырья.
Пектинэстераза (Н.Ф.3.1.1.11). Пектинэстеразы синтезируются высшими растениями, микроскопическими грибами, дрожжами и бактериями. Пектинэстераза катализирует гидролиз сложноэфирных связей в молекуле растворимого пектина, в результате чего образуется метиловый спирт и полигалактуроновая кислота. Процесс протекает согласно следующей схеме (стрелками показано действие фермента):
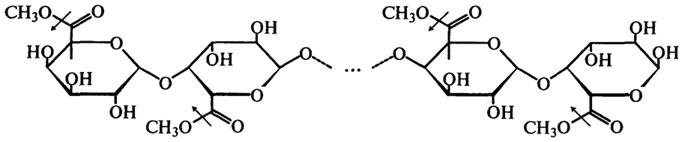
Таким образом, пектинэстераза отщепляет метоксильные группы от метоксилированной полигалактуроновой кислоты (см. также гл. Углеводы).
Желирующая способность пектина зависит от степени метоксилирования или степени этерификации, поэтому действие пектинэстеразы по отщеплению метоксильных групп приводит к снижению желирующей способности и сопровождается падением вязкости. На этом, очевидно, и основывается применение этого фермента для осветления плодовых соков и вина. Обычно комплексные препараты пектолитических ферментов, применяемые для этих целей, получают из различных плесневых грибов, и прежде всего из A. niger.
Гидролазы гликозидов или гликозидазы (Н.Ф.3.2).Этот подкласс включает около ста ферментов с разной специфичностью действия, осуществяющих гидролиз олиго- и полисахаридов; некоторые ферменты этого типа способны осуществлять трансферазные реакции — переносить гликозидные остатки на олиго- и полисахариды, наращивать полисахаридные цепочки. Представители гликозидаз были одними из первых ферментов, обратимость действия которых in vitro была экспериментально доказана.
Основной формой запасных углеводов в семенах и клубнях растений является крахмал. Ферментативные превращения крахмала лежат в основе многих пищевых технологий. Поэтому ферменты амилолитического комплекса растительного, животного и микробного происхождения интенсивно изучаются со времени их открытия Кирхгофом в 1814 г. и до настоящего времени.
α-Амилаза (Н.Ф.3.2.1.1). α-Амилазы обнаружены у животных (в слюне и поджелудочной железе), в растениях (проросшее зерно пшеницы, ржи, ячменя), они вырабатываются плесневыми грибами и бактериями. Все эти ферменты гидролизуют крахмал, гликоген и родственные α-1,4-глюканы с образованием, главным образом, декстринов и небольшого количества дисахарида — мальтозы.
α-Амилазы гидролизуют α-1,4-связи внутри молекулы крахмала, разрывая связь между первым углеродным атомом и кислородом, связывающим этот углерод с соседней молекулой глюкозы. Это наглядно демонстрирует следующая схема (стрелками показано действие фермента):

Скорость, с которой α-амилазы гидролизуют глюканы различной степени полимеризации, быстро уменьшается по мере ее снижения. Амилоза — линейная фракция крахмала, гидролизуется быстрее, чем амилопектин, имеющий разветвленную структуру.
Скорость гидролиза α-амилазой зависит от вида и состояния крахмала (нативный или клейстеризованный крахмал), а также от эффективности самих амилаз. На основании параллельно проводившихся опытов (в одних — действовали препаратами амилаз на клейстеризованный крахмал, а в других — эквивалентными концентрациями на нативные крахмальные зерна) было показано, что эффективность амилаз различного происхождения уменьшается в следующем порядке: панкреатическая, солодовая, бактериальная, грибная.
Характерной особенностью всех α-амилаз является наличие одного атома Са на молекулу фермента. Роль кальция состоит в том, что он стабилизирует вторичную и третичную структуру молекулы α-амилазы, обеспечивая таким образом ее каталитическую активность и вместе с тем предохраняя фермент от действия протеолитических ферментов и тепловой денатурации.
Различные α-амилазы отличаются по молекулярной массе, устойчивости к нагреванию и некоторым другим показателям. Молекулярная масса α-амилаз близка к 50 000 Да, за исключением бактериальной α-амилазы, которая имеет молекулярную массу 96 900 Да (кристаллический препарат). Так, например, широко применяемая в промышленности α-амилаза из плесневого гриба A. oryzae, полученная в кристаллическом виде, имеет молекулярную массу 51 860 Да.
Большое практическое значение имеет влияние температуры и рН на стабильность амилаз. Быстрое разрушение зерновой α-амилазы при рН 3,3 — 4,0, например, дает возможность выпекать ржаной хлеб из муки, которая содержит избыток α-амилазы, при низких значениях рН, чтобы предотвратить излишнее декстринирование крахмала и образование клейких веществ в мякише хлеба.
Говоря о термостабильности α-амилаз различного происхождения, можно расположить их в следующем ряду по мере снижения устойчивости к нагреванию: бактериальные амилазы — зерновые амилазы — грибные амилазы.
Последними работами в области изучения амилаз показано, что в семенах растений присутствуют два типа α-амилазы: α-амилаза созревания и α-амилаза прорастания.
В созревающем зерне синтезируется α-амилаза созревания, которая затем переходит в латентную форму, локализуясь на мембранах алейронового слоя. Первый этап гидролиза крахмала при прорастании осуществляется этой α-амилазой. И только на следующем этапе в работу включается вновь синтезируемый фермент — α-амилаза прорастания. Ее синтез в клетках зародыша и алейронового слоя начинается при влажности зерна выше 28%. Две формы α-амилазы семян злаков различаются по термостабильности: α-амилаза созревания при 70°С теряет 50% своей активности, тогда как α-амилаза прорастания при этой температуре только незначительно снижает свою активность.
Интенсивность гидролиза крахмала в перерабатываемом сырье, как уже отмечалось ранее, определяется взаимодействием многих факторов. Это прежде всего состояние амилаз созревшего зерна и возможность перехода части латентной формы в свободное состояние. Это и состояние субстрата, его доступность действию фермента (атакуемость субстрата). Большое значение имеет и фракционный состав крахмальных гранул, соотношение мелких и крупных зерен, а также содержание поврежденных зерен крахмала, которые легче поддаются действию ферментов.
Как было установлено в последнее время, важная роль в этом процессе принадлежит протеолитическим ферментам. Протеазы, осуществляя ограниченное расщепление белков, способствуют освобождению амилаз из связанного состояния, а также гидролизуют ту часть запасных белков, которая прочно связана с поверхностью крахмальных гранул, облегчая тем самым доступ фермента к субстрату.
Мощным механизмом регуляции скорости расщепления крахмальных гранул является система белковых ингибиторов амилаз, широко представленных в растениях. Ингибиторы белковой природы избирательно взаимодействуют с амилазами и образуют неактивные комплексы "амилаза — ингибитор". Высокой активностью обладают ингибиторы амилаз картофельного сока. Из зерна пшеницы выделен ингибитор с двумя активными центрами (двухцентровой). Один активный центр имеет сродство к протеазам и способен блокировать их действие. Другой активный центр имеет сродство к амилазам. Таким образом, один ингибитор белковой природы способен блокировать работу как протеаз, так и амилаз. В образующемся надмолекулярном комплексе ингибитор выполняет своеобразную роль связывающего звена, подавляя активность ферментов разного механизма действия.
β-Амилаза (Н.Ф.3.2.1.2). β-Амилаза отщепляет мальтозу от нередуцирующего конца цепи, разрывая гликозидные связи через одну. Название "|3-амилаза" было выбрано для того, чтобы показать, что мальтоза образуется в β-аномерной форме. Это не означает, что в молекуле крахмала присутствуют β- связи, а указывает скорее на то, что происходит инверсия конфигурации, которая может иметь место в процессе ферментативного превращения вещества, содержащего асимметрический атом углерода. Такая инверсия была открыта П. Вальденом в 1893 г. и поэтому названа вальденовской инверсией. На представленной ниже схеме действие β-Амилазы на амилозу и амилопектин показано стрелками.
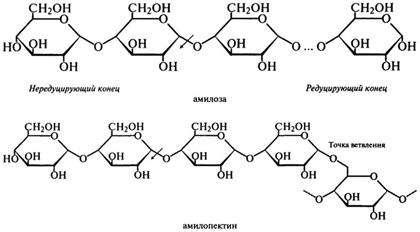
Таким образом, действуя упорядочение, β-Амилаза последовательно отщепляет остатки мальтозы с нередуцирующего конца до тех пор, пока не встретится точка ветвления со связью α-1,6. При этом амилоза под действием β-Амилазы расщепляется до мальтозы на 100%, а при действии β-Амилазы на амилопектин помимо образующейся мальтозы остается нетронутой крупная, сильно разветвленная сердцевина, так называемый "конечный декстрин", т. к. фермент прекращает свое действие за 2 — 3 остатка глюкозы от точек ветвления.
β-Амилазы — это ферменты в основном растительного происхождения. Хорошо известными источниками являются зерно пшеницы, а также пшеничный и ячменный солод, соевые бобы, клубни картофеля.
В отличие от α-амилазы, β-Амилаза менее термостабильна, но проявляет большую устойчивость к кислым значениям рН, сохраняя свою активность при рН 3,3. Это нашло свое отражение в способе разделения α-и β-Амилаз солода, где оба фермента присутствуют одновременно.
Глюкоамилаза (Н.Ф.3.2.1.3). Глюкоамилаза (у-амилаза) продуцируется различными видами плесневых грибов рода Aspergillus: A. oryzae, A. niger, A. awamory и некоторыми другими, например, Rhizopusdelamarn Rhizopus niveus. Эти ферменты расщепляют как амилозу, так и амилопектин до глюкозы, последовательно действуя с нередуцирующего конца цепи крахмала. Они способны гидролизовать α-1,4 и α-1,6 гликозидные связи.

Различные глюкоамилазы отличаются друг от друга скоростью гидролиза крахмала, отношением к температуре и рН, и некоторыми другими показателями. На использовании препаратов грибной глюкоамилазы разработан ферментативный метод получения глюкозы, который получил широкое распространение в Японии.
Поллуланаза(Н.Ф. 3.2.1.41). Ранее этот фермент был известен под другими названиями — R-фермент, предельная декстриназа, дебранчинг-фермент.
Поллуланаза является эндогенным ферментом, она способна хаотично гидролизовать α-1,6-гликозидные связи в пуллулане, амилопектине, гликогене и предельных декстринах, которые получаются при совместном воздействии на крахмал и гликоген α- и β-Амилаз. Наиболее частым отцепляемым фрагментом является мальтотриоза. На представленной ниже схеме действие пуллулоназы на пуллулан показано стрелками.

Продуцетами пуллуланазы являются Aerobacter aerogenes, Bacillus cereus, Bacillus polimyxa, Bacillus sp. и Streptomyces. Ферменты, полученные из различных источников, обладают разной молекулярной массой (от 48 000 до 143 000 Да) и по разному относятся к температуре и рН, действию ингибиторов и активаторов.
Инулаза (Н.Ф. 3.2.1.7). Фермент осуществляет гидродиз инулина и других полифруктозанов по (3-1,2-фруктозидной связи, начиная с β-фруктозидного конца полимера. В результате образуется фруктоза и единственная молекула глюкозы на одну молекулу инулина. При полном гидролизе инулина получается 95% фруктозы и 5% глюкозы.
Фермент гидролизует главным образом инулин; сахароза, рафиноза также гидролизуются, но с незначительной скоростью. Инулаза содержится в тех же растениях (топинамбур, цикорий), в которых присутствует инулин. Активная инулаза продуцируется Aspergillus awamori BKM-808 при глубинном культивировании. Препарат обладает высокой стабильностью к Н+-ионам и температуре. Оптимум рН действия 4,5; оптимум температуры — 65°С.
Полученные из инулина фруктозные сиропы могут быть широко использованы в кондитерской промышленности и диетическом питании.
β-Фруктофуранозидаза (Н.Ф.3.2.1.26). Другие названия этого фермента — инвертаза или сахараза.
Для промышленного производства имеют значения только ферменты из S. cerevisiae и S. carlsbergensis. β-Фруктофуранозидазу выделяют из дрожжей путем автолиза. Этот фермент гидролизует сахарозу по β-фруктозидной связи согласно уравнению:

В результате действия фермента на сахарозу получается смесь эквимолярных количеств α-глюкозы и β-фруктозы, получившая название "инвертного сахара". Термин "инверсия" обозначает изменения, происходящие в способности сахара вращать плоскость поляризованного света. Это можно выразить следующей схемой:
Сахароза + Н2О → D (+)-глюкоза + D ( — )-фруктоза
[α]D=+66,5° [ α]D = +52,5° [α]D = -92,4°
Оптимум рН дрожжевой инвертазы находится в достаточно широкой зоне от 4,0 до 5,5. Фермент ингибируется ионами металлов. Полное ингибирование происходит под действием ртути и свинца; частичное ингибирование вызывают ионы серебра, цинка, меди. β-Фруктофуранозидаза гидролизует также рафинозу и метил-β-О-фруктофуранозид, причем, если относительную скорость гидролиза сахарозы принять за 100, то соответствующие скорости расщепления этих субстратов будут равны 47 и 77.
Инвертаза находит широкое применение в пищевой промышленности. Гидролиз концентрированных растворов сахарозы приводит к образованию более сладких сиропов. Точка кипения инвертированных сиропов выше, а точка замерзания ниже, т. к. при инверсии повышается осмотическое давление. Образовавшиеся при действии инвертазы моносахариды более растворимы, не так легко выкристаллизовываются из высококонцентрированных сиропов. Практическое использование инвер
Последнее изменение этой страницы: 2016-08-28
lectmania.ru. Все права принадлежат авторам данных материалов. В случае нарушения авторского права напишите нам сюда...