
Категории:
ДомЗдоровьеЗоологияИнформатикаИскусствоИскусствоКомпьютерыКулинарияМаркетингМатематикаМедицинаМенеджментОбразованиеПедагогикаПитомцыПрограммированиеПроизводствоПромышленностьПсихологияРазноеРелигияСоциологияСпортСтатистикаТранспортФизикаФилософияФинансыХимияХоббиЭкологияЭкономикаЭлектроника
Вращение плоскости поляризации света
Если пропускать через вещество плоско поляризованный свет, то ориентация плоскости поляризации может измениться — повернуться на некоторый угол относительно исходного положения. Вещества, вызывающие такой эффект, называются оптически активными. Их отличительная особенность — определенная асимметрия геометрической формы молекул, а именно: в точечной группе симметрии не должно быть операций отражения (s). Такие молекулы нельзя совместить с их отражениями в зеркале и поэтому они существуют в виде двух энантиомерных форм (или конфигураций). Наглядным примером могут служить органические молекулы, содержащие хотя бы один т.н. асимметрический атом углерода (С*) — такой, у которого все четыре заместителя различны.
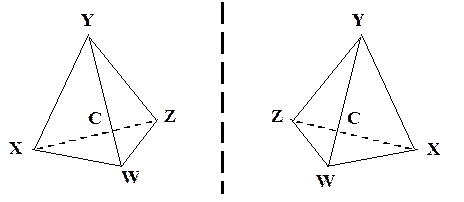
В зависимости от направления поворота плоскости поляризации света различают правовращающие (+) и левовращающие (–) оптически активные вещества (если смотреть навстречу пучку света, то правый поворот соответствует повороту по часовой стрелке, левый — против часовой стрелки)

Как меру оптической активности вещества можно рассматривать величину угла поворота a. Обычно в качестве характеристики вещества используют т.н. удельное вращение — угол поворота относят к единичной концентрации раствора c и единичной толщине слоя веществаl:
[a] = a / cl
Удельное вращение зависит от температуры, длины волны света, используемого растворителя. Поэтому все эти характеристики указывают в справочниках вместе с величиной удельного вращения.
Метод анализа, основанный на измерении оптической активности веществ, называется поляриметрией. Его применимость ограничена, поскольку далеко не все вещества являются оптически активными. Это ограничение, однако, можно преодолеть. Если поместить оптически не активное вещество в сильное магнитное поле, форма его молекул искажается нужным образом, и вещество приобретает оптическую активность (эффект Фарадея).
Существенное значение имеет тот факт, что оптическая активность вещества зависит от длины волны света. Эта зависимость называется эффектом Коттона или дисперсией оптического вращения (ДОВ). Она носит индивидуальный характер для разных веществ, что позволяет использовать спектры ДОВ для идентификации веществ и изучения их строения. Соответствующая разновидность поляриметрии называется методом спектрополяриметрии.
Эллиптическая поляризация света
При отражении плоско поляризованного света от поверхности твердого тела (жидкости) он приобретает т.н. эллиптическую поляризацию. Параметры эллипса поляризации отраженного света зависят от строения молекул на поверхности вещества. Это позволяет использовать данный эффект для изучения строения поверхностей, явлений адсорбции и т.д. (эллипсометрия).
Резонансные взаимодействия
Резонанс наблюдается при совпадении энергии световых квантов с разностями между энергиями соседних стационарных состояний атомов и молекул:
hn = DE
При резонансе наблюдается поглощение света веществом, так что в результате интенсивность падающего света при некоторых (резонансных) частотах снижается и образуется спектр поглощения. Исследование спектров поглощения — спектроскопия — является наиболее эффективным и результативным средством изучения строения атомов и молекул. Существует множество разновидностей спектроскопии, различаемых:
по природе объектов:
2 ядерная
2 электронная
2 атомная
2 молекулярная
по области электромагнитного спектра:
2 радиоспектроскопия
2 микроволновая,
2 инфракрасная (ИК-)
2 оптическая,
2 ультрафиолетовая (УФ-)
2 рентгеновская,
2 гамма-спектроскопия
по природе квантовых переходов
2 магнитно-резонансная (ЯМР- и ЭПР-)
2 вращательная
2 колебательная
2 электронная
2 фотоэлектронная
2 ядерная гамма-резонансная (ЯГР-)
Все разновидности спектроскопии имеют специфические возможности и применяются для решения различных аналитических и структурных задач.
При фиксированной частоте поглощение света пропорционально количеству молекул (вещества). Это дает возможность применения явления поглощения света для целей количественного анализа — определения содержания химических соединений в различных смесях (фотометрия).
Поглощение света часто сопровождается рядом дополнительных эффектов, среди которых можно выделить следующие.
Резонансная флуоресценция. Поглощенный квант света через определенное время (Dt ~ 10–8 c) испускается наружу. Частота света при этом сохраняется.

Комбинационное рассеяние. Так же, как и в предыдущем случае, поглощенный квант света через определенное время (Dt ~ 10–8 c) испускается наружу, однако его частота изменяется. Наряду с основной полосой флуоресцентного рассеяния, в излученном свете наблюдаются дополнительные частоты пики (сателлиты), частота которых немного отличается от исходной (n** = n* ±Dn).
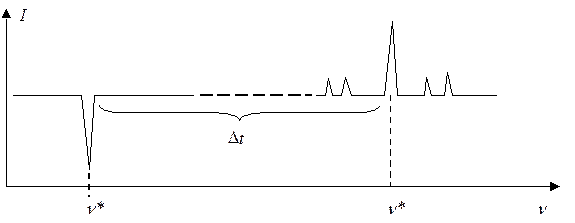
Причиной изменения частоты являются колебательные и вращательные переходы молекулы, сопровождающие переходы электронов.
Флуоресценция и фосфоресценция. Поглощенный свет испускается наружу, но с существенно меньшей частотой и с временной задержкой (~ 10–8 c в случае флуоресценции и ~ 10–4 c в случае фосфоресценции). Причиной снижения частоты является участие промежуточных электронных уровней.
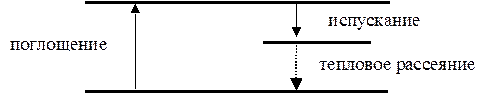
Все эти эффекты, сопровождающие обычное резонансное поглощение света зависят от внутреннего строения молекул и поэтому могут быть использованы для исследования ее строения. Они лежат в основе различных видов эмиссионной спектроскопии: флуоресцентной, комбинационного рассеяния (КР-) и др.
Если энергия квантов падающего света превышает некоторый предел, могут также наблюдаться различные фотоэффекты.
Ионизация молекулы, сопровождающаяся вылетом одного или нескольких электронов. Измерение кинетической энергии вылетевших фотоэлектронов позволяет найти энергию их связи внутри молекулы (атома), и, следовательно, оценить установить энергии молекулярных (атомных) орбиталей. Этот эффект лежит в основе метода рентгеновской фотоэлектронной спектроскопии (РФЭС), которую иногда называют методом электронной спектроскопия для химического анализа (ЭСХА).
Гомолиз химических связей, в ходе которого молекула распадается на два свободных радикала или образует бирадикал.
H3C—H ¾® H3C• + •H
H2C=CH2 ¾® H2C•—•CH2
Этот эффект позволяет использовать облучение молекул светом (обычно УФ- или g-излучение) для инициирования разнообразных химических реакций.
Последнее изменение этой страницы: 2016-08-28
lectmania.ru. Все права принадлежат авторам данных материалов. В случае нарушения авторского права напишите нам сюда...