
Категории:
ДомЗдоровьеЗоологияИнформатикаИскусствоИскусствоКомпьютерыКулинарияМаркетингМатематикаМедицинаМенеджментОбразованиеПедагогикаПитомцыПрограммированиеПроизводствоПромышленностьПсихологияРазноеРелигияСоциологияСпортСтатистикаТранспортФизикаФилософияФинансыХимияХоббиЭкологияЭкономикаЭлектроника
Переробка і продукти переробки твердого палива
ЗМІСТ
1. Переробка і продукти переробки твердого палива
2. Сучасні технології хімічної переробки бурого вугілля
3. Значення продуктів палива в народному господарстві
4. Переробка нафти
5. Переробка природного газу
6. Застосування продуктів перегонки природного газу
Висновки
Список використаних джерел
СУЧАСНІ ТЕХНОЛОГІЇ ХІМІЧНОЇ ПЕРЕРОБКИ БУРОГО ВУГІЛЛЯ
Переробка твердого палива у рідке є складним процесом, оскільки для його реалізації необхідно розруйнувати макромолекулу на простіші рухливі фрагменти. Ця задача вирішується за допомогою трьох традиційних напрямків (рис. 1.1): прямим приєднанням водню під тиском – гідрогенізація; піролізом, що супроводжується розподіленням водню між рідкими продуктами і твердим залишком, і газифікацією вугілля водяним паром з отриманням суміші СО і Н2 та синтезом з неї рідких продуктів. Останню застосовують також для отримання водню.

Рис. 1.1 – Схема отримання рідких продуктів із вугілля.
У 1950-х рр. відкриті багаті родовища нафти у СРСР, на Близькому Сході та в інших районах світу. Це обумовило призупинку досліджень і виробництва синтетичного рідкого палива з вугілля, так як його вартість була в 5-7 разів вищою вартості моторного палива, одержаного з нафти. В 1970-х рр. ціна на нафту різко підвищилася і невпинно росте до сьогодні. Водночас, стало очевидним, що при існуючих масштабах споживання нафти (~3 млрд. т/рік) запаси її, придатні для видобутку традиційними свердловинними методами, будуть виснажені до середини XXI ст. Проблема залучення твердого палива, головним чином вугілля, у переробку для одержаннях рідких продуктів-замінників нафти стала знову актуальною.
Піроліз
Під термічною переробкою вугілля (піролізом) розуміють процеси, що відбуваються при нагріванні вугілля у відсутності реагентів. Термічна переробка твердих палив застосовується для одержання облагороджених вуглецевих твердих матеріалів, а також рідких і газоподібних продуктів. Залежно від призначення продуктів вихідною сировиною може бути практично будь-яке вугілля. Як правило, термічну переробку вугілля ведуть при відсутності каталізаторів; відсутні також складні системи рециркуляції, що визначає достатню простоту апаратурного оформлення. У зв'язку із цим питомі капітальні витрати на термічну переробку значно нижчі, ніж у інших процесах переробки вугілля з одержанням твердих, рідких і газових продуктів.
Процеси термічної переробки вугілля почали застосовуватися вже наприкінці XVIII - початку XIX століття (виробництво кам'яновугільного коксу, одержання облагородженого вугілля для бездимного спалювання, виробництво світильного газу та ін.) Значна частина процесів термічної переробки палив, що використовуються у наші дні, особливо коксохімічне виробництво, сформувалася в результаті тривалої еволюції технічних і апаратурних рішень і відрізняється відносно сприятливими витратами, енергетичними й екологічними показниками.
У той же час варто враховувати й певні обмеження, що накладаються на процеси термічної переробки вугілля. Всі вони відносно мало селективні, особливо при переробці найпоширенішого і дешевого гумусового вугілля. У будь-яких варіантах процесу одночасно одержують тверді, газоподібні й рідкі багатокомпонентні продукти склад, яких обумовлюється елементним складом вихідного вугілля. Рідкі продукти термічної переробки твердих горючих копалин містять велику кількість органічних сполук, що містять кисень, азоті сірку, і тому не можуть бути безпосередньо використані як синтетичне рідке вуглеводневе паливо. Тому термічна переробка вугілля не може розглядатися як самостійний спосіб приготування штучних рідких палив.
Гідрогенізація
Гідрогенізація вугілля – перетворення високомолекулярних речовин органічної маси вугілля (ОМВ) під дією водню на рідкі й газоподібні продукти при 400-500°С у присутності різних речовин-органічних розчинників, каталізаторів і т.п. Наукові основи цього процесу були розроблені на початку XX століття В.М. Іпатьєвим, М.Д. Зелінським, Ф. Бергіусом, Ф. Фішером та ін. У 30-х рр. XX ст. у деяких країнах, зокрема у Німеччині і Великобританії, були побудовані промислові підприємства для одержання з вугілля й смол бензину, дизельного палива, мастильних масел, парафінів, фенолів і т.п. В 1940-х рр. виробництво рідких продуктів з вугілля перевищувало 4 млн. т/рік. В 1950-х рр. гідрогенізація вугілля була освоєна у напівпромисловому масштабі у СРСР. Одна з найпоширеніших схем гідрогенізації показана на рис. 1.2.

Рис 1.2 – Схема отримання синтетичного рідкого палива з вугілля
Для гідрогенізації вугілля застосовують неокиснене буре і малометаморфізоване кам'яне вугілля. Вміст мінеральної частини в них не повинен перевищувати 5-6%, відношення С : Н - 16, вихід летких речовин повинен бути більшим за 35%, вміст петрографічних компонентів групи вітриніту й ліптиніту - більш ніж 80%. Високозольне вугілля необхідно попередньо піддавати збагаченню.
Органічна маса вугілля з вмістом С – 63-71%, що зазвичай застосовується для гідрогенізації, являє собою самоасоційований мультимер, що складається із просторово структурованих блоків (олігомерів). Блоки включають макромолекули з атомів вуглецю, водню і гетероатомів (О, N, S), що обумовлює нерівномірний розподіл електронної щільності, тому в блоках здійснюється донорно-акцепторна взаємодія, у т.ч. утворюються водневі зв'язки. Енергія розриву таких зв'язків не перевищує 30 кДж/моль. Розрізняють блоки з молекулярною масою 200-300, 300-700 і 700-4000, розчинні відповідно у гептані (масла), бензолі (асфальтени) і піридині (асфальтоли). Усередині блоків макромолекули зв'язані метиленовими, а також О-, N- і S-утримуючими містками. Енергія розриву цих зв'язків в 10-15 разів більше енергії розриву блоків. При гідрогенізації вугілля в першу чергу відбувається роз'єднання блоків. Наступна деструкція блоків вимагає підвищення температури, присутності активного Н2. Для одержання з вугілля рідких продуктів необхідно поряд з деструкцією здійснити гідрування низькомолекулярних неорганічних сполук, що утворюються.
Для підвищення реакційно здатної поверхні вугілля подрібнюють до крупності менше 0,1 мм, часто об'єднуючи цей процес із сушкою. Кращі результати досягаються при вібропомолі й подрібненні у дезінтеграторі. Зовнішня питома поверхня при цьому зростає в 20-30 разів, об'єм перехідних пор - в 5-10 разів. Відбувається механохімічна активація поверхні, у результаті чого підвищується реакційна здатність вугілля. Важливе місце займає сушка. Волога, що заповнює пори, перешкоджаючи проникненню у вугільну речовину реагентів, виділяється в ході процесу в реакційній зоні, знижуючи парціальний тиск Н2, а також збільшує кількість стічних вод. Вугілля сушать до залишкового вмісту вологи 1,5%, використовуючи трубчаті парові сушарки, вихрові камери, труби-сушарки, у яких теплоносієм служать гарячі топкові гази з мінімальним вмістом О2 (0,1-0,2%), щоб вугілля не піддавалося окисненню. Щоб уникнути зниження реакційної здатності вугілля не нагрівають вище ніж 150-200 °С.
Для збільшення ступеня перетворення ОМВ в рідкі продукти на поверхню вугілля наносять каталізатор (з розчинів солей, у вигляді порошку, емульсії або суспензії) у кількості 1-5% від маси вугілля. Чим активніший каталізатор, тим при нижчому тиску може бути здійснена гідрогенізація вугілля. Максимальною каталітичною активністю володіють сполуки Mo, W, Sn, при використанні яких гідрогенізацію вугілля можна проводити при відносно низькому тиску - 10-14 МПа. Однак їхнє застосування обмежене через труднощі регенерації з суміші із залишком непереробленого вугілля. Тому в багатьох процесах застосовують дешеві, хоча й малоактивні, каталізатори (наприклад, так званий червоний шлам-відходи після виділення А12О3 з бокситів), компенсуючи їхню недостатню активність підвищенням тиску водню до 30-70 МПа. У значній мірі на процес впливає хімічний склад і властивості розчинника-пастоутворювача, у суміші з яким (50-60% пастоутворювача) вугілля піддається переробці. Пастоутворювач повинен містити висококиплячі фракції продукту гідрогенізації вугілля (точка кипіння > 325 °С) з мінімальним вмістом асфальтенів для утримання вугілля в рідкій фазі. У більшості варіантів гідрогенізації вугілля до пастоутворювача додають речовини з водневодонорними властивостями для стабілізації блоків, що утворюються з вугільного мультимера при відносно низькій температурі (200-350о С), коли молекулярний водень малоактивний. Блоки легко від'єднують водень у донорів і завдяки цьому не "злипаються". Водневодонорний компонент пастоутворювача одержують гідруванням фракції гідрогенізації вугілля із точкою кипіння 300-400°С. У цьому випадку бі-, три- і тетрациклічні ароматичні вуглеводні частково гідруються з утворенням гідроароматичних похідних, які здатні віддавати водень з вищими швидкостями, ніж нафтенові вуглеводні. Кількість донорів у пастоутворювачі може становити 20-50% (сполука пастоутворювача оптимізується залежно від виду сировини й умов гідрогенізації). В якості донора використовують також висококиплячі фракції нафтопродуктів. Ступінь перетворення ОМВ підвищується при введенні у пастоутворювач органічних додатків - сполук, здатних вступати у взаємодію з вугіллям і продуктами його деструкції ( в-піколін, хінолін,антрацен, нафталін та ін.). Додатки також тимчасово стабілізують реакційно здатні радикали, що утворюються при первинній деструкції вугілля, і в такий спосіб перешкоджають утворенню побічних продуктів конденсації.
Отриману вуглемасляну пасту в суміші із циркулюючим воденьвмісним газом (80-85% Н2 на вході, 75-80% - на виході) нагрівають у системі теплообміну трубчатої печі і потім направляють на гідрогенізацію в реактор. На 1 т пасти вводять 1,5-5,5 тис. м3 газу. Частину газу подають у реактор холодним для охолодження реакційної суміші й підтримки постійної температури, оскільки при гідрогенізації вугілля виділяється 1,2-1,6 МДж на 1 кг вугілля. При зростанні температури збільшується швидкість деструкції ОМВ, однак одночасно зменшується швидкість гідрування.
Гідрогенізацію здійснюють у трьох або чотирьох послідовно розташованих циліндричних пустотілих реакторах. Тривалість гідрогенізації вугілля, як правило, визначається об'ємною швидкістю подачі вуглемасляної пасти в реакційну систему. Ця швидкість залежить від типу вугілля, пастоутворювача, каталізатора, температури й тиску процесу. Оптимальна об'ємна швидкість підбирається емпірично й становить, як правило, 0,8-1,4 т на 1 м3 реакційного об'єму за годину (розробляються процеси з вищою об'ємною швидкістю).
Продукти реакції розділяють у сепараторі на парогазову суміш і важкий залишок - шлам. З першого потоку виділяють рідкі продукти (масло, воду) і газ, який після відділення насичених вуглеводнів (С 1- С 4), NH3, H2S, CO2 і С, Н2O збагачують 95-97%-ним Н2 і повертають у процес. Шлам розділяють на рідкі продукти й твердий залишок. Рідкі продукти після видалення води піддають дистиляції на фракцію з температурою кипіння до 325-400 °С і залишок, що повертають у процес для приготування пасти. У зв'язку зі складною будовою ОМВ, різною реакційною здатністю її фрагментів кінцеві рідкі продукти містять багато компонентів, переважно моно- і біциклічні ароматичні й гетероцикліні сполуки з домішками парафінових і нафтенових вуглеводнів, а також феноли, піридинові основи й інші речовини, які можуть бути виділені.
Вуглеводневі гази деструктивної гідрогенізації вугілля і важких нафтових залишків, на відміну від газів деструктивної переробки нафтопродуктів, характеризуються практичною відсутністю в їх складі ненасичених вуглеводнів. Це пояснюється тим, що цей процес протікає в умовах високих концентрацій водню, що у присутності каталізаторів зумовлює цілковите насичення неграничних зв'язків вуглеводнів, які утворюються. Гази деструктивної гідрогенізації вугілля, після вилучення з них аміаку, сірководню і відмивання вуглекислоти, є дуже багатою сировиною для одержання зріджених газів. Крім газів ароматизації, ці газові суміші містять зовсім незначну кількість неграничних вуглеводнів.
Газифікація
При високотемпературній обробці твердого палива в середовищі кисню повітря, водяної пари, діоксиду вуглецю і водню органічні складники палива повністю перетворюються в газоподібні продукти. Сьогодні освоєні різні модифікації промислових процесів газифікації вугілля, найпоширенішими з яких є технології Лургі (стаціонарний шар грудкового вугілля), Вінклера (киплячий шар вугільних частинок), Копперс-Тотцека (пиловугільний потік), Тексако (водновугільна суспензія). Ефективність процесів газифікації може істотно підвищуватися при використанні відповідних каталізаторів, що дозволяють знижувати температуру при збереженні високої швидкості процесу й регулювати склад продуктів.
Вплив каталізатора на процес газифікації твердого палива.
Каталізатор може прискорювати як реакції прямого перетворення вуглецю в газоподібні сполуки, так і газофазні реакції продуктів термічного перетворення вугілля. Дотепер переважно розробляли процеси каталітичної газифікації, засновані на прискоренні реакцій прямого перетворення вугілля в газоподібні сполуки. У цих випадках для ефективного впливу каталізатора необхідно забезпечити його добрий контакт із твердою сировиною. Для цього використовують каталізатори, що наносяться на поверхню вугілля, а також здатні плавитися або переганятися в умовах процесу, проникаючи у пори вугілля. Найпоширенішими каталізаторами процесу газифікації вугілля є сполуки лужних, лужноземельных і деяких перехідних (Ni, Fe, Co) металів. Найбільш розповсюдженими технологіями газифікації є: процес ЕКСОН - каталітична газифікація вугілля водяною парою в киплячому шарі, процес МОЛТЕН СОЛТ - парокиснева газифікація при підвищеному тиску в розплаві соди, процес ПАТГАЗ - газифікація при атмосферному тиску в розплаві заліза. Застосовувані розплави відіграють роль теплоносія й каталізатора.
Застосування каталізаторів може викликати нові технологічні проблеми. Серед них варто виділити проблему розробки простих і надійних методів введення каталізатора в реакційну суміш і виведення його для повторного використання в процесі газифікації. Ця проблема може вирішуватися шляхом здійснення процесу газифікації вугілля в киплячому шарі часток каталізатора. Виявилося, що як каталітично активні матеріали можна використовувати дешеві й доступні металургійні і котельні шлаки, які містять елементи (Fe, Ni, Mn і ін.), здатні каталізувати реакції окиснення, конверсії СО і вуглеводнів, метанування. Такі каталітично активні матеріали можна використовувати в процесі газифікації до їхнього повного зношення. У режимі циркуляції частинок мартенівських шлаків при температурах 850 – 900°C і атмосферному тиску пароповітряної суміші ступінь конверсії вугілля в газоподібні продукти становить 90%, а інтенсивність газифікації перевищує показники відомих технологій газифікації, здійснюваних при аналогічних температурах і тиску.
Переробка нафти
Методи переробки нафти.Розрізняють первинні і вторинні методи переробки нафти.
Первинні (фізичні) методи засновані на різних температурних інтервалах кипіння окремих фракцій нафти – це прямий відгін нафти.
Вторинні (хімічні) методи засновані на повному перетворенні нафтової сировини під дією підвищеної температури і тиску, а також застосування каталізаторів; це різні види крекінгу і риформінгу нафти.
Усі методи засновані на високотемпературних ендотермічних процесах і реакціях, тобто для їхнього здійснення необхідне підведення тепла ззовні.
Первинна переробка нафти (прямий відгін нафти). У промислових умовах перегонка нафти здійснюється одноразовим випарюванням із подальшою ректифікацією, при якій відбирають наступні світлі фракції: бензинову (до
180 °С), газову (120-315 °С), дизельну чи газо-газойлеву (180-350 °С) і різні проміжні відгони. Світлі фракції за допомогою наступного очищення, змішання, а іноді і після вторинного перегону перетворюються в продукти прямої перегонки нафти.
До світлих товарних нафтопродуктів прямої перегонки відносять бензин (автомобільний і авіаційний), розчинник у лакофарбовому виробництві, що заміняє скіпідар, ("уайт-спірит"), розчинник для гумової промисловості, екстракційний, петролейний ефір, лігроїн (приладовий), газ (освітлювальний, для технічних цілей). Мазут переробляється перегоном під вакуумом для одержання масляних фракцій.
Дистиляційні олії (авіаційні, автомобільні, дизельні, індустріальні і білі), що утворюються після перегону мазуту, відбираються за в'язкістю, а не за температурою кипіння і густиною.
Залишок після перегону мазуту (вище 500 °С) називається гудроном, чи напівгудроном у залежності від в'язкості. Використовуються вони для готування високов'язких мастил, будівельних і дорожніх нафтових бітумів. «Залишковими оліями» називають продукти, що одержують з гудронів екстракцією органічними розчинниками
Перегкою нафти називають процес її термічного поділу на частини (фракції) без помітного розкладання вуглеводнів, що входять до складу нафти. Здійснюють на одно- або двоступінчатих установках. У одноступінчатих установках перегонку проводять за атмосферним тиском з одержанням моторних палив і мазуту, що застосовується як паливо.
Більш раціональне застосування двоступінчатих установок:
- на першій стадії при атмосферному тиску одержують моторні палива і мазут;
- на другій стадії при зниженому тиску виділяють із мазуту мастила і гудрон, що перероблюється в пек, асфальт, нафтовий кокс. Перегонку ведуть під вакуумом, щоб не відбувалося розщеплення важких вуглеводнів.
Термічні процеси переробки. У залежності від умов і призначення поділяються на:
- термічний крекінг;
- піроліз;
- коксування.
Так як, нафта складається з великого числа індивідуальних вуглеводнів, при високих температурах будуть протікати різноманітні реакції. Поряд з термічним розпадом будуть здійснюватися реакції синтезу, ізомеризації, причому багато з цих реакцій – оборотні.
Для деструктивної переробки нафтової сировини характерні наступні реакції: дезалкілування (скорочення бічних парафінових ланцюгів), полімеризація, циклізація алкенів (алкени в сировині відсутні, але утворюються при дегідруванні алканів), дециклизація (утворюються ароматичні вуглеводні), розпад моноциклічних вуглеводнів на алкани й алкени.
Деструктивна перегонка нафти (крекінг) (вторинні або хімічні методи переробки). У результаті первинної переробки нафти з неї виділяють у виді окремі фракції речовини, що входять у її склад. Використання деструктивних методів дозволяє одержувати нові речовини, що є товарними продуктами, необхідними для різних галузей народного господарства.
Процеси крекінгу поділяються на:
1) термічні – процеси розщеплення вуглеводнів під дією високих температур і тиску;
2) термокаталитичні – процеси, які протікають під впливом температури в присутності каталізаторів.
Переваги термокаталітичних процесів:
- протікають з більшою швидкістю при більш низьких температур і тиску, за рахунок застосування каталізаторів;
- збільшується вихід коштовних продуктів, підвищується їхня якість за рахунок застосування селективних каталізаторів;
- можливість одержання продуктів заданого складу.
Термічний крекінг. Як сировина для крекінгу служать різні фракції: газойль, солярка, газ, мазут, гудрон, а також бензин прямого перегону нафти. Різні види сировини доцільно піддавати крекінгу окремо, підбираючи для кожного процесу відповідні умови.
Термічний крекінг здійснюється за двома основними варіантами: у рідкій фазі (тиск 2-7 МПа, температура 450-500 °С) і в паровій фазі (тиск 0,2 - 0,5 МПа, температура 550-600 °С). При рідкофазному крекінгу більший вихід бензину і менше газу, ніж при парофазному крекінгу.
Термічні перетворення вуглеводнів. З алканів утворюються нижчі алкени та алкани.Метан починає перетворюватися лише за 1000 °С, етан – 500 °С, пропан – 450 °С. Для вищих вуглеводнів при t > 400 °С розпад по С–С зв’язку стає головним. Крекінг н-бутану відбувається за такою схемою:
1) ініцюювання:
2CH3-·CH2
CH3CH2CH2CH3 ·CH3+CH3-CH2-·CH2
2) продовження ланцюга по 2-м напрямкам:
а) b-розпад великих радикалів:
·CH3+CH2=CH2
СН3СН2-·СH2
·H+CH3CH=CH2
б) заміщення стійких до розпаду радикалів:
H·(·CH3, ·C2H5)+C4H10 H2(CH4, C2H4)+·C4H9
3) створенний бутильний радикал вступає в реакцію b-розпаду:
CH3-CH2-CH2-·CH2 ·C2H5+CH2=CH2
CH3-CH2-·CH-CH3 ·CH3+CH2=CH-CH3
Сумарна схема деструкції бутану:
СH4+CH2=CHCH3
С4Н10 C2H6+CH2=CH2
Термічний розпад вищих алканів (С6 та більше) зі збільшенням глибини перетворення пришвидшується у зв’язку з наявності алкенів, маючих слабкий С–С зв’язок в b-положенні до С=С.
Для нафтенів більш можливі реакції розпаду циклоалканів до елементів та дегідрування до дієнів та аренів. Швидкість розпаду по С–С набагато більша, ніж С–Н. Головні продукти крекінгу – алкани та алкени, дієни та Н2.
CH2 3CH2=CH2
H2C CH2 CH2=CH-CH2-CH2CH2-CH3
CH2=CH2+CH2=CH-CH2-CH3
H2C CH2
C2H6+CH2=CH-CH=CH2
CH2
Реакції йдуть також по радікальному механізму через бі-радикал, який з’являється при ініціюванні.
Перетворення аренів термодинамічно можливо за реакціями: розпад до елементів; розкриття ароматичного кільця (при великій t 0С).
При робочих температурах йде тільки дегідроконденсація:
2C6H6 C6H5–C6H5+H2
Розпад відбувається швидше по боковим алкільним ланцюгам за реакцією
b-розпаду. Основні напрямки – крекінг алканових ланцюгів та дезалкілювання таким чином, продуктами термічного перетворення аренів є стирол, алкани та інші продукти крекінгу бокових ланцюгів толуолу, бензолу. Перетворюються також алкени, котрі створюються з основних продуктів.
Внаслідок того, що в практиці крекінгу піддаються складні суміші і виходять продукти дуже складного хімічного складу, важко встановити безпосередній зв'язок між компонентами сировини й одержуваними продуктами. Швидкість крекінгу в однакових умовах зростає з підвищенням температури кипіння вихідних нафтових фракцій. У сумішах швидше всього піддаються крекінгу термічно менш стійкі високомолекулярні алкани й арени з довгими бічними ланцюгами.
Швидкість реакцій крекінгу, кількість і якість одержуваних продуктів залежать від температури, складу сировини, тривалості крекінгу при заданій температурі, а також тиску в реакційній зоні. При термічному крекінгу одночасно протікають реакції термічного розкладання з поглинанням тепла і реакції ущільнення, з виділенням тепла, але тому що сумарний тепловий ефект негативний, необхідно підводити теплоту ззовні.
Основні, продукти термічного крекінгу:
1) вуглеводневий газ (етан, пропан, етилен, пропилен), служить сировиною для органічного синтезу;
2) крекінг-бензин, характеризується низьким октановим числом;
3) гасо-газойлева фракція, використовується як дизельне паливо;
4) термогазойль, використовується для виробництва технічного вуглецю;
5) крекінг-залишок (казанове паливо), його якість краще, ніж якість прямогонного мазуту (більш висока теплота згоряння, більш низькі температура замерзання і в'язкість).
Піроліз. Основне призначення процесу піролізу вуглеводневої сировини - одержання нижчих алкенів. Процес проводять при 700-1000 °С під тиском, близьким до атмосферного.


У промислових умовах для виробництва етилену і пропілену проводять піроліз нафтових фракцій. Найбільш високий вихід етилену досягається при піролізі легких бензинів парафінової групи з великим вмістом вуглеводнів нормальної будови. Поряд з етиленом і алкенами С3 - С4 утворюється значна кількість рідких продуктів, що містять алкени, циклоалкени, алкадієни С5 і вище, а також арени С6-С8 і ін. компоненти. Вихід продуктів при піролізі різних бензинів складає (% мас): етилен 22 – 32; пропілен 10 –17; фракція С4 – 5-12, арени 6-13.
Коксування нафтових залишків. Процес глибокого розкладання нафтових фракцій без доступу повітря з метою одержання нафтового коксу і рідкого палива (бензин, газойль) при температурі 400-500°С.
Коксування дозволяє утилізувати залишки, такі як мазут, гудрони, асфальти, крекінг–залишок. Промислові процеси коксування поділяють на три типи: безперервні, напівбезперервні і періодичні. Найбільше поширення на сьогодні має напівбезперервний процес в установках уповільненого коксування, що протікає при 505-515°С під тиском 0,2-0,3 МПа. У результаті коксування крім нафтового коксу одержують бензин, газ, середні і важкі коксові дистиляти, вихід і якість яких залежить від хімічного і фракційного складу сировини.
Термокаталитичні процесивключають:
- каталітичний крекінг;
- каталітичний риформинг;
- гідрокрекінг.
Каталізатори, використовувані в цих процесах, повинні характеризуватися наступними показниками:
- високорозвиненою поверхнею;
- високою активністю;
- стійкістю до контактних отрут;
- підвищеною механічною міцністю, тому що процес ведуть у зваженому шарі або в потоці каталізатора, що рухається, тобто в умовах тертя зерен одне об одне;
- простота регенерації, тому що в процесі крекінгу поверхня каталізатора дуже швидко блокується шаром коксу.
Каталітичний крекінг. Для проведення процесу використовуються синтетичні алюмосиликатні каталізатори, які містять у своєму складі цеоліти: алюміний, кремній,лужні метали.
Особливість крекінгу: швидка дезактивація каталізатору (пори каталізатору закоксовуються через 10-15 хвилин роботи). Тому крекінг чергується з регенерацією. Вона полягає в випалюванні коксу і смолистих відкладень з поверхні катализатору повітрям при температурі 550-600°С. Для зберігання каталізатору від локальних перегрівів повітря розбавляють інертним газом.
Від складу сировини залежить:
- дезактивація каталізатору;
- вихід рідких і газоподібних продуктів.
Тому із сировини, що надходить на крекінг, видаляють сірчисті сполуки, які знижують активність каталізатору.
Вихід продуктів крекінгу залежить від часу зіткнення реакційної маси з каталізатором. Зі збільшенням часу контакту збільшується ступінь перетворення сировини й одночасно вихід газів, бензину і коксу.
З підвищенням температури вихід бензину збільшується за рахунок розкладання важких вуглеводнів, потім вихід зменшується, тому що відбувається розщеплення легких вуглеводнів з утворенням газів. Тому температура процесу 450-500 °С. Кокс, що утворюється, дезактивує каталізатор. Регенерований каталізатор знову повертається в реактор.
Контакт сировини з каталізатором здійснюється:
– у щільному шарі каталізатора, що рухається зверху вниз;
– в зваженому шарі каталізатора;
– у висхідному потоці суспензії каталізатора.
Недолік установки крекінгу з щільним шаром каталізатора, що рухається: неповне використання внутрішньої поверхні зерен каталізатора. Тому широке поширення одержали установки крекінгу в киплячому шарі. У цих апаратах година перебування каталізатору в зоні реакції складає 1,5-6 хв. Реактор крекінгу в киплячому шарі складається з двох зон: зони каталізу і зони регенерації - розташованих над зоною каталізу.
Каталітичний риформінг. Використовується для підвищення октанового числа бензинових фракцій і для одержання аренів. У процесі риформінгу молекули вуглеводнів піддаються перебудові без зміни числа вуглецевих атомів у молекулі.
В основі процесу лежать реакції:
- дегідрування циклоалканів в арени;
- дегідроциклізація алканів.
При риформингу протікають побічні процеси:
- крекінг вищих вуглеводнів з утворенням газоподібних алканів і алкенів;
- дегідроконденсація ароматичних вуглеводнів
Вихід аренів росте з підвищенням температури і зниженням тиску. Так як реакція дегідроконденсації оборотна, риформінг проводять під тиском водню, що запобігає виділенню коксу і збільшує термін служби каталізатора.
Температура риформінгу залежить від застосовуваного каталізатора:
1) каталізатори на основі осидів хрому і молібдену. Процес ведуть при температурі 480-550°С, під тиском водню 1,5-2,5 МПа.
2) алюмо-платиновий каталізатор (найбільш розповсюджений). Підвищення вмісту платини в каталізаторі збільшує його активність і приводить до збільшення октанового числа бензину. З іншого боку, зі збільшенням вмісту платини прискорюють реакції з утворенням метану і розщеплення циклоалканів, що зменшує вихід бензину. Ці каталізатори дуже чуттєві до сульфатних і азотних сполук, домішок свинцю, миш'яку, вологи. Тому сировину очищують й осушують. Процес ведуть при температурі 470-540 °С, тиску 2-4 МПа в атмосфері газу, що містить водень.
Основні продукти риформингу:
– газ, що містить водень використовується частково для відшкодування витрат газу, а більша частина направляється на установки гідрокрекінгу і гідроочищення нафтопродуктів;
– риформат використовується як автомобільний бензин або направляється на виділення аренів.
Гідрокрекінг. Гідрогенізаційний крекінг (деструктивна гідрогенізація) дозволяє одержувати значну кількість легких продуктів при використанні як сировини важких нафтових дистилятів, важких нафт, нафтових залишків – малоцінних мазутів. При цьому процесі одержують бензин, дизельне і котлове паливо.
Процес протікає в одну чи в дві стадії (у випадку важкої сировини). Двостадійний процес включає рідку фазу гідрогенізації (температура 420-500 °С, тиск 3-10 МПа, каталізатор – суспензія оксиду заліза (III)), у результаті якої одержують у невеликих кількостях газ і бензин, а в основному – широку фракцію (200-350 °С), що служить сировиною для другої стадії – парової фази гідрогенізації.
Парова фаза гідрогенізації (температура 380-420 °С, тиск до 10 МПа, каталізатори – сульфіди й оксиди металів, а також Pt, Pd на алюмосилікатах) дозволяє одержувати бензин, гас, газойль і газ, що включає головним чином залишковий водень, якого витрачається 1–3 %. Бензин гідрогенізації з напівгудрону грозненської нафти складається в основному з алканів (47–70 %), нафтенів (26- 36 %), аренів (3-10 %) і невеликої кількості олефінів і має октанове число менше 70.
Переробка природного газу
Природні горючі (вуглеводневі) гази умовно поділяються на власне природні, тобто гази, що добуваються з чисто газових родовищ, і попутні, що добуваються попутно з нафтою у нафтогазових родовищах.
Усі супутні гази належать до жирних газів, тому що в їхньому складі, крім метану, міститься значна кількість етану, пропану, бутану й ін.
До природного газу належать і супутні гази, які розчинені у нафті, містяться над нею і виділяються під час її добування. На поверхню нафта поступає під тиском цих газів і фонтанує. Супутній нафтовий газ відрізняється за складом від природного: у ньому містить менше метану (30-59% за об’ємом), але більше етану, пропану, бутану, пентану (7-20% за об’ємом) і вищих вуглеводнів, ніж у природному газі.
Під час переробки супутного нафтового газу (рис.) спочатку відокремлюють рідкі легко киплячі вуглеводні – пентан, гексан та ін. Вони разом утворюють так званий газовий бензин (газолін), який використовується як добавка до звичайних бензинів для кращого їх займання під час запуску двигунів.
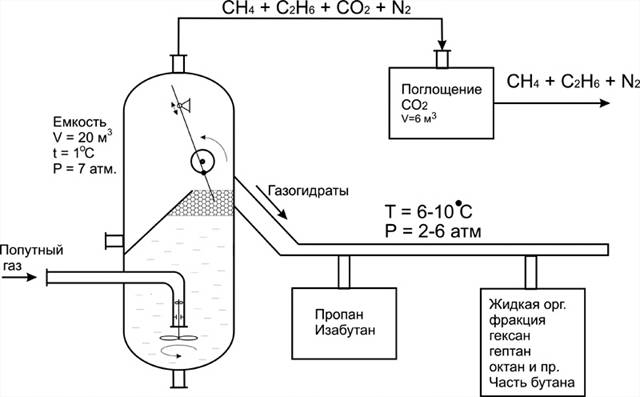
Рис. Переробка супутного нафтового газу.
Потім відокремлюється пропан – бутанова суміш, якою заповнюють балони під тиском. Зріджений газ використовується як газоподібне паливо, що залишається після відокремлення газового бензину і бутан-пропанової суміші, складається переважно з метану і використовується як паливо.
Для хімічної переробки з супутнього газу відокремлюють індивідуальні вуглеводні: етап, пропан, н-бутан тощо. Оскільки насичені вуглеводні відносно хімічно інертні і мало придатні як сировина для хімічного синтезу, їх перетворюють за допомогою реакцій.
Переробка попутних нафтових жирних газів. У схемах перегонки нафти вторинної перегонки бензинової фракції на інших установках відгоняють головну фракцію НК–65°С, яка вміщує (у середньому) СН 4-6%, С2 – 5,4%, С3 –19,7%, С4–66%, С5–1,4%, крім того, компоненти бензину С5-С6. подібні газові фракції С1–С4 відділяються в бензинових газосепараторах. Такі фракції скраплюють під тиском 1-3МПа, але значна їх кількість залишається у вигляді газу, який називають жирним газом. Він вміщує С1–12%, С2–10%, С3–25%, С4–52%. Це основні компоненти, крім них жирний газ вміщує вуглеводні С5–С6 (в меншій кількості).
Для відділення бензину із жирних газів використовують абсорбційний метод за допомогою неполярного абсорбента–бензинової фракції при температурах 30–40°С чи нижче 0°С з використанням холодних установок. Таким чином зменшується кількість газу–головна фракція – до 10% від сировини (нафти), сухий газ – 1–2%. Процес деетанізації-відділення газів С2–С3 чи дебутанізаці С1–С4 проводять у фракционіруючому абсорбері.
На ОНПЗ на деетанізаціюспрямовують вуглеводвеві гази та фракції НК-
62 °С з атмосферної перегонки нафти, вуглеводневих газів та фракція НК-62 з установки каталітичного ріформінгу. Здобувають сухий газ–23,5 %, фракція С3 – 18,5 %, фракція н-С4 16,9 %, фракція ізо-С4 11,1 %, фракція С5 – 30 %.
ВИСНОВКИ
Паливом називають існуючі в природі чи штучно отримані речовини, що є джерелом теплової енергії та сировиною для хімічної промисловості.
Природне паливо:
тверді – вугілля, деревина, сланці, торф;
рідкі – нафта;
газоподібні – природні та попутні гази.
Штучне паливо одержують головним чином під час переробки природного палива. Тверде штучне паливо – кокс, напівкокс, деревне вугілля; рідке – бензин, гас, нафта та ін; газоподібне – генераторні гази, коксовий газ, гази переробки нафти та ін.
Вугілля – це тверда горюча копалина органічного походження, що утворилася з вимерлих рослин і планктону в результаті діяльності мікроорганізмів.
Дрова – це деревина, яка після заготовки розпилюється на потрібний розмір, складується для просушування і згодом використовуються для спалювання в котлах.
Деревні брикети – це пресована деревина та відходи деревообробки, що виробляється промисловим сектором.
Пелети – це спеціальне паливо, сформоване в зручну для транспортування, зберігання та застосування форму, яке зазвичай використовується для автоматичної подачі в опалювальне устаткування
Торф є найменш сформованою формою вугілля, що досить сильно зберегла риси рослинного походження і складається з води (до 90%), Карбону (5%) та летких сполук (5%). Залягає він переважно на болотах
Горючі сланці – цінний вид палива й хімічної сировини, що складається з органічної (від 10-30 до 50-70% ) і мінеральної (глинистої, кременистої та ін.) масових частин.
Переробка твердого палива у рідке є складним процесом, оскільки для його реалізації необхідно розруйнувати макромолекулу на простіші рухливі фрагменти. Ця задача вирішується за допомогою трьох традиційних напрямків (рис. 1.1): прямим приєднанням водню пі
Последнее изменение этой страницы: 2016-07-22
lectmania.ru. Все права принадлежат авторам данных материалов. В случае нарушения авторского права напишите нам сюда...