
Категории:
ДомЗдоровьеЗоологияИнформатикаИскусствоИскусствоКомпьютерыКулинарияМаркетингМатематикаМедицинаМенеджментОбразованиеПедагогикаПитомцыПрограммированиеПроизводствоПромышленностьПсихологияРазноеРелигияСоциологияСпортСтатистикаТранспортФизикаФилософияФинансыХимияХоббиЭкологияЭкономикаЭлектроника
Кондуктометрическое титрование смеси хлороводородной и уксусной кислот (работа № 16)
Цель работы: определение количества HCl и CH3COOH в растворе при совместном присутствии методом кондуктометрического титрования.
Сущность метода. Кондуктометрические методы анализа основаны на измерении электропроводности растворов. Кондуктометрическое титро-вание используется при определении концентраций индивидуальных веществ и разнообразных смесей. Точку экивалентности находят по изменению электропроводности раствора. Зависимость электропровод-ности раствора от объема добавленного титранта изображают графически. Полученный график называется кривой кондуктометрического титрования. Излом на кривой соответствует точке эквивалентности.
Оборудование: 1) кондуктометр OK-102/1; 2) магнитная мешалка; 3) стаканы на 300 см3 (ячейки для титрования) – 2 шт.; 4) штатив для бюреток; 5) бюретки на 25 см3 с воронками – 3 шт. (для растворов соляной и уксусной кислот, гидроксида натрия); 6) стакан на 300 см3 с делениями или мензурка; 7) кристаллизатор для промывания электрода; 8) промывалка.
Реактивы: 1) 0,5 н. раствор гидроксида натрия (20 г/дм3); 2) 0,1 н. раствор уксусной кислоты; 3) 0,1000 н. раствор хлороводородной кислоты (готовят из фиксанала, растворяя содержимое одной ампулы (0,1 моль) в мерной колбе на 1 дм3).
Ход работы. Приготовление раствора гидроксида натрия и опреде-ление его концентрации. Готовят ~0,5 н. раствор NaOH, растворяя 20 г гид-роксида натрия (взвесить на технических весах) в 1 дм3 дистиллированной воды. Полученный раствор заливают в бюретку. В ячейку отмеряют пипет-кой 10,00 см3 0,1000 н. раствора HCl, доливают дистиллированную воду, чтобы отверстия на электроде были погружены в раствор. Включают магнитную мешалку и через 1 – 2 мин проводят измерение начальной электропроводности раствора (порядок проведения измерений см. ниже). Раствор в ячейке титруют из бюретки раствором NaOH порциями по 1 см3. После добавления каждой порции перед измерением электропроводности выжидают 1 – 2 мин. Результаты измерений заносят в табл. 2.5.
Таблица 2.5
Титрование раствора соляной кислоты кондуктометрическим методом (V(HCl) = 10,00 см3; Сн(HCl) = 0,1000 моль/дм3)
| Титрование 1 | Титрование 2 | Титрование 3 | |||
| V(NaOH), см3 | 1/R, Ом –1 | V(NaOH), см3 | 1/R, Ом –1 | V(NaOH), см3 | 1/R, Ом –1 |
| … | … | … | … | … | … |
Строят график зависимости электропроводности от объема раствора NaOH (рис. 2.14). По резкому перегибу на кривой находят точку эквива-лентности, определяют эквивалентный объем титранта Vэкв(NaOH).

Рис. 2.14. Зависимость электропроводности раствора соляной кислоты от объема прилитого раствора гидроксида натрия
Первое титрование можно провести с повышенной скоростью, приливая по 2 см3 титранта. При последующих титрованиях вблизи точки эквивалентности порции титранта уменьшают до 1,0 – 0,5 см3. После точки излома определяют электропроводность еще в 4 – 5 точках. Титрование повторяют до получения трех сходящихся (т.е. различающихся не более чем на 0,1 см3) результатов. Из трех параллельных определений находят среднее значение эквивалентного объема раствора гидроксида натрия 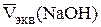 и рассчитывают концентрацию NaOH с точностью до четырех значащих цифр:
и рассчитывают концентрацию NaOH с точностью до четырех значащих цифр:
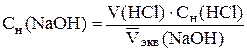 .
.
Определение концентрации уксусной кислоты. Титруют 10,00 см3 ~0,1 н. раствора уксусной кислоты. Задача выполняется точно так же, как при титровании раствора HCl. Титрование повторяют до получения трех сходящихся результатов. Результаты заносят в таблицу, аналогичную табл. 2.5. Графически определяют эквивалентный объем NaOH, рассчиты-вают среднее арифметическое 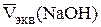 и концентрацию уксусной кислоты с точностью до четырех значащих цифр:
и концентрацию уксусной кислоты с точностью до четырех значащих цифр:

Учебная задача. При ее выполнении студенты проверяют правиль-ность своей работы. Самостоятельно составить смесь кислот, для чего от-мерить пипеткой в ячейку некоторые объемы растворов HCl и CH3COOH (например, 11,00 и 12,00 см3). Полученную смесь титруют раствором NaOH. На кривой титрования наблюдается 2 излома (рис. 2.15).

Рис. 2.15. Кривая кондуктометрического титрования смеси хлороводородной и уксусной кислот
Точки эквивалентности 1 и 2 соответствуют изломам на кривой титрования. После аппроксимации линейных участков прямыми и опреде-ления точек их пересечения (см. приложение 3) находят эквивалентные объемы раствора гидроксида натрия, пошедшие соответственно на титрование HCl V1(NaOH) и CH3COOH V2(NaOH). Поскольку до первой точки эквивалентности титруется только HCl, то
V1(NaOH) = Vэкв1
После первой точки эквивалентности титруется слабая уксусная кислота, поэтому
V2(NaOH) = Vэкв2 – Vэкв1
Рассчитывают исходные объемы хлороводородной и уксусной кислот с точностью до четырех значащих цифр:
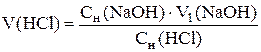

Если экспериментально найденные значения объемов кислот совпадают с исходными (допустима относительная ошибка 0,2 – 0,3%), то можно приступить к контрольной задаче.
Контрольная задача. Получить задачу у инженера лаборатории. Перенести ее количественно в ячейку. Провести титрование. Построить кривую титрования, как и в учебной задаче. Рассчитать объемы кислот в исследуемом растворе. Зная объемы и концентрации, рассчитать содержание кислот в исходной смеси в г/дм3. По результатам трех параллельных определений рассчитать среднеквадратичную ошибку и доверительный интервал для полученных величин (доверительная вероят-ность 95%).
Задание
1. Построить кривые титрования, найти точки эквивалентности, опре-делить эквивалентные объемы для каждого титрования (см. приложение 3).
2. Рассчитать концентрацию раствора гидроксида натрия.
3. Рассчитать концентрацию раствора уксусной кислоты.
4. Рассчитать объемы стандартных растворов хлороводородной и ук-сусной кислот в контрольной задаче.
5. Рассчитать массу HCl и СH3СООН в контрольной задаче.
6. Рассчитать концентрации растворов HCl и СH3СООН в контрольной задаче (в г/дм3).
7. При наличии нескольких параллельных измерений проводят ста-тистическую обработку результатов анализа: рассчитывают среднее арифметическое значение, среднеквадратичную ошибку, доверительный интервал, относительную ошибку определения (см. приложение 2).
Порядок проведения измерений на кондуктометре ОК-102/1:
1. Включить прибор в сеть.
2. Обеспечить уровень раствора выше отверстия на корпусе электрода.
3. Нажать красную кнопку на приборе, чтобы загорелась лампочка.
4. Установить ручку «Range» в положение, когда стрелка находится в середине шкалы. Если стрелка зашкаливает в ту или иную сторону, следует изменить положение данной ручки.
5. Нажать черную кнопку и ручкой «Calibration» установить стрелку на 15 по нижней шкале или на 5 по верхней в зависимости от положения ручки «Range». Повторить настройку 3 – 4 раза.
6. Начать титрование. После добавления порции титранта замерять электропроводность анализируемого раствора по соответствующей шкале.
Контрольные вопросы
1. Сущность метода. Принципиальная схема прибора.
2. Какой стандартный раствор используется в данном методе анали-за? Как он готовится? Расчет навески для приготовления 500 см3 0,5 н. раствора NaOH. На каких весах надо брать навеску? Какая мерная посуда требуется для приготовления раствора? Как определяется его точная концентрация?
3. Приготовление стандартного раствора HCl.
4. Как приготовить и определить точную концентрацию раствора ук-сусной кислоты?
5. Какое значение в данном методе анализа играет подвижность ионов? Какие ионы обладают наибольшей подвижностью? В чем суть «эстафетного» механизма переноса заряда ионами Н+ и ОН–?
6. Какие процессы происходят в системе при титровании раствором гидроксида натрия смеси соляной и уксусной кислот? Объясните кондуктометрические кривые. Почему при титровании уксусной кислоты электропроводность не падает, а растет?
7. Как определяется точка эквивалентности в кондуктометрическом титровании?
8. Почему возможно определение смеси кислот кондуктометричес-ким методом?
9. Эквивалентная и удельная электропроводность. Какая из них из-меряется в ходе анализа?
10. В каких единицах измеряется электропроводность?
11. Какие электроды используются в анализе? Их устройство.
12. Постоянный или переменный ток проходит через ячейку?
13. Достоинства и недостатки метода.
14. Как рассчитать массу HCl и CH3COOH в контрольной задаче?
15. Способы выражения концентрации растворов.
Последнее изменение этой страницы: 2016-07-23
lectmania.ru. Все права принадлежат авторам данных материалов. В случае нарушения авторского права напишите нам сюда...