
Категории:
ДомЗдоровьеЗоологияИнформатикаИскусствоИскусствоКомпьютерыКулинарияМаркетингМатематикаМедицинаМенеджментОбразованиеПедагогикаПитомцыПрограммированиеПроизводствоПромышленностьПсихологияРазноеРелигияСоциологияСпортСтатистикаТранспортФизикаФилософияФинансыХимияХоббиЭкологияЭкономикаЭлектроника
Моль. Закон Авогадро. Мольный объем газа.
Контрольные задания:
1.Сколько молекул содержится в 1,00 мл водорода при нормальных условиях.
2.Какой объем при нормальных условиях занимают 27 ∙ 1021 молекул газа?
3.Определить объем, занимаемый 0,07 кг при 21 0С и давлении 142 кПа (1065 мм рт. ст.).
4.Оксид углерода (IV) находится в сосуде, объем которого равен 20 л, при температуре 22 0С и давлении 500 кПа. Определите массу оксида углерода (IV).
5.Сколько молей содержится в 20 мл газа при 300 К и давлении 103 кПа?
6.Вычислите массу 10 л водорода при температуре 291 К и давлении 101,3 кПа.
7.Вычислите объем метана массой 3 кг при температуре 320 K и давлении 102 кПа.
8.Найдите массу углекислого газа в колбе объемом 250 мл при 300 К и давлении 102 кПа.
9.Определите объем, который займет при нормальных условиях газовая смесь, содержащая водород массой 1,4 г и азот массой 5,6 г.
10.Какой объем Н2 (при 17 0С и давлении 102,4 кПа) выделится при растворении 1,5 кг цинка в соляной кислоте?
11.Смесь состоит из 92 г этанола и 72 г воды. Определите количество атомарного кислорода в смеси.
12.Какую массу имеет образец гидроксосульфата алюминия количеством вещества 0,2 моль?
13.Определите массу образца воды, содержащего 12,04×1022 молекул воды.
14.Определите массу раствора этанола в воде, содержащего 12,04×1022 атомов углерода и 24,08×1022 атомов кислорода.
15.Какой объем (н.у.) занимает оксид углерода (II) массой 5,6 г?
16.Какую массу имеет образец гидрофосфата калия количеством вещества 0,5 моль?
17.Газообразное соединение (НХ) занимает объем, равный 6,72 л (н.у.). Его масса равна 6 г. Определите Х.
18.Газовая смесь, состоящая из фтора и гелия, имеет молярную массу 21 г/моль. Определите объем гелия при н.у. в смеси массой 4,2 г.
19.Смесь состоит из 80 г пропанола и 60 г воды. Определите количество атомарного кислорода в смеси.
20.Определите массу 11,2 л водорода при н.у.
21.Привести объем газа к нормальным условиям, если при температуре 300ºС и давлении 1,8кПа он равен 1,5м3
22.Выразить в единицах массы, а также, для газообразных веществ, - в единицах объема: а) 0,3 моль азотной кислоты; б) 2 моль углекислого газа (н.у.)
23.Выразить в молях: а) 5,6дм3 водорода (н.у.); б) 10кг оксида бария.
24.Выразить в единицах массы, а также, для газообразных веществ, - в единицах объема: а) 5 моль ацетилена (С2Н2) (н.у.); б) 10 моль гидроксида марганца (II).
25.Выразить в молях: а) 11,2м3 кислорода (н.у.); б) 10г хлорной кислоты.
26.Вычислить массу 1м3 азота при 10ºС и давлении 102,9кПа.
Тема № 5.
Строение атома.
Представления о строение атома необходимо при изучении периодического закона Д.И.Менделеева, химической связи и свойств соединений. Без знания строения атома невозможно материалистическое понимание химических и биологических наук.
Основные понятия и определения.
| Атом | - электронейтральная микросистема, состоящая из положительно заряженного ядра и отрицательно заряженных электронов. |
| Атомное ядро | - частица, расположенная в центре атома, состоит из протонов, имеет положительный заряд, равный числу протонов. |
| Массовое число | -сумма протонов (Z) и нейтронов (N), входящих в состав ядра: А = Z+ N. |
| Элемент | -совокупность атомовс одинаковым зарядом ядра. |
| Изотопы | -разновидности одного и того же химического элемента,отличающиеся массой атома. |
| Атомная орбиталь (АО) | -область околоядерного пространства, в котором наиболее вероятно нахождения электрона. |
| Квантовые числа | - характеристики состояния электрона в атома. |
| Энергетический уровень | -состояние электрона в атоме, характеризующеесяопределенным значением главного квантового числа n |
| Энергетический подуровень | -состояние электрона в атоме, характеризующееся определенными значениями квантовых чисел n и l |
| Основное состояние атома | - состояние атома с наименьшей энергией; электрон в основном состоянии связан с ядром наиболее прочно |
| Возбужденное состояние атома | - состояние с высоким уровнем энергии; при возбуждении атома связь электрона с ядром ослабевает |
| Валентные электроны | -электроны, принимающие участие в образовании химических связей |
Характеристика квантовых чисел:
| Квантовые числа | Возможные значения | Число значений | Определяют |
| Главное n | 1,2,3… 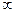
| 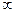
| основной запас энергии электрона, размеры электронного облака, энергетический уровень |
| Орбитальное l | 0,1,2,3… (n-1) | n | форму электронного облака, энергетический подуровень |
| Магнитное m | -1,…,0,…,+1 | 2l+1 | Пространственную ориентацию электронного облака |
| Спиновое s | ±1/2 | Собственный момент количества движения электрона |
Последовательность заполнения электронами АО в соответствии с правилами Клечковского:
| Тип орбитали | Главное квантовое число n | Орбитальное квантовое число l | n + l | Тип орбитали | Главное квантовое число n | Орбитальное квантовое число l | n + l | |
| 1s | 5p | |||||||
| 2s | 6s | |||||||
| 2p | 4f | |||||||
| 3s | 5d | |||||||
| 3p | 6p | |||||||
| 4s | 7s | |||||||
| 3d | 5f | |||||||
| 4p | 6d | |||||||
| 5s | 7p | |||||||
| 4d |
Пример 1. Составьте электронную формулу атома элемента с порядковым номером 16. Покажите расположение электронов этого атома по энергетическим ячейкам.
Решение. Электронные формулы отображают распределение электронов в атоме по энергетическим уровням, подуровням (атомным орбиталям). Электронные конфигурации обозначаются группами символов n  х, где n – главное квантовое число,
х, где n – главное квантовое число,  –орбитальное квантовое число (вместо него указывают соответствующее буквенное обозначение s, p, d, f), х – число электронов в данном подуровне (орбитали). При этом следует учитывать, что электрон занимает тот энергетический подуровень, на котором обладает наименьшей энергией – меньшей суммой n+
–орбитальное квантовое число (вместо него указывают соответствующее буквенное обозначение s, p, d, f), х – число электронов в данном подуровне (орбитали). При этом следует учитывать, что электрон занимает тот энергетический подуровень, на котором обладает наименьшей энергией – меньшей суммой n+  (правило Клечковского). Последовательность заполнения энергетических уровней и подуровней следующая:
(правило Клечковского). Последовательность заполнения энергетических уровней и подуровней следующая:
1s→2s→2p→3s→3p→4s→3d→4p→5s→4d→5p→6s→5d1→
→4f→5d→6p→7s→6d1-2→5f→6d→7p.
Так как число электронов в атоме того или иного элемента равно его порядковому номеру в таблице Менделеева, то для элемента № 16 (сера) электронная формула будет иметь вид: 1s22s22p63s23p4.
Электронная структура атомов может быть изображена также в виде схемы размещения электронов в квантовых (энергетических) ячейках, которые являются схематическими изображениями атомных орбиталей (АО), квантовую ячейку изображают в виде прямоугольника или линейки, а электроны в этих ячейках обозначают стрелками. В каждой квантовой ячейке может быть не более двух электронов с противоположными спинами ↑↓ (принцип Паули).
Орбитали данного подуровня заполняются сначала по одному электрону с одинаковыми спинами, а затем по второму электрону с противоположными спинами (правило Хунда).
Контрольные задания:
1.Напишите электронные формулы атомов фосфора и меди. Укажите, к какому электронному семейству относится каждый из элементов, и определите число протонов и нейтронов в ядре их атомов.
2.Укажите последовательность заполнения электронами атомных орбиталей 4d, 5s, 6s, 5р и сформулируйте правило, определяющее эту последовательность.
3.Напишите электронно- графические формулы атомов элементов с порядковыми номерами 15 и 27. определите число нейтронов и электронов в их атомов.
4.В соответствии с принципом Паули укажите максимальное число электронов на s-, р-, d-, f- подуровнях данного энергетического уровня.
5.Дайте определение понятия изотоп. Объясните причину нецелочисленных значений атомных масс большинства химических элементов. Вычислите атомную массу серебра, если известно, что массовые доли изотопов в природном серебре составляют соответственно 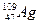 - 40% и
- 40% и 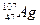 - 60%.
- 60%.
6.Дайте определения понятия s-, р-, d-, f- элемент. Приведите примеры.
7.Энергетическое состояние электрона в атоме описывается четырьмя квантовыми числами n, l, m, s.укажите, какие значения может принимать каждое из них. Определите набор квантовых чисел для внешнего электрона атома натрия.
8.Составьте электронные формулы атомов элементов с порядковыми номерами 17 и 25. Укажите, к какому электронному семейству относится каждый из них. Приведите электронные и электронно - графические формулы атомов элементов II периода, которые могут иметь на р – подуровне один электрон, учитывая как основное, так и возбужденное состояние атома.
9.Укажите число квантовых d – орбиталей в основном состоянии у атомов элементов с порядковыми номерами 23, 42, 47, 49.
10.Составьте электронные формулы атомов элементов с порядковыми номерами 14, 25 и укажите, к какому электронному семейству они относятся.
11.Объясните физический смысл главного и орбитального квантовых чисел и укажите, какие значения они принимают.
12.Объясните физический смысл магнитного квантового числа и укажите, какие значения оно может принимать при данном числовом и буквенном значении орбитального квантового числа. Заполните таблицу:

| m | |
| Числовое значение | Буквенное значение | |
| s | ||
13.Напишите электронную формулу элемента, в атоме которого содержится один электрон на 3d – орбитали. Укажите период, группу и символ этого электрона.
14.Приведите формулы, позволяющие рассчитать электронную емкость энергетического уровня и подуровня, а также число орбиталей на данном уровне и подуровне.
15.Сформулируйте правило Клечковского. Определите порядок заполнения электронами орбиталей 3d, 4s, 4р, 5s, 5р.
16.Укажите период, группу и символ химического элемента, атому которого соответствует электронная формула: [Ne ] 3s2 3р6 3d5 4s2. К какому электронному семейству он относится?
17.Укажите возможные значения квантовых чисел для электронов второго и третьего энергетических уровней. Заполните таблицу:
| n | 
| m | s |
18.Укажите число протонов и нейтронов в ядре атома углерода, изотопа  . Напишите электронную формулу атома углерода в основном и возбужденном состояниях.
. Напишите электронную формулу атома углерода в основном и возбужденном состояниях.
19.Напишите электронные формулы атомов элементов с порядковыми номерами 8 и 24. Подчеркните валентные электроны и укажите, к какому электронному семейству относится каждый элемент.
20.Назвать элементы, имеющие по одному электрону на подуровне: а) 3d; б) 4d; в) 5d. Написать электронные формулы атомов этих элементов и указать их положение в периодической системе – период, группа и подгруппа.
21.Сколько свободных d-орбиталей имеется в атомах титана и ванадия? Написать для них электронно-графическую структуру d-подуровня.
22.Назвать элементы 4-го периода, атомы которых содержат наибольшее число непарных d-электронов. Написать электронно-графическую структуру их d-подуровня.
23.Написать электронно-графические формулы атомов индия, германия и титана в нормальном и возбужденном состоянии.
24.У элементов каких периодов электроны внешнего слоя характеризуются значением n + l = 5?
25.Указать порядковый номер элемента, у которого: а) заканчивается заполнение электронами орбиталей 4d; б) начинается заполнение подуровня 4р.
26.Сколько вакантных 3d-орбиталей имеют возбужденные атомы: а) Сl; б) V; в) Mn?
27.Среди приведенных ниже электронных конфигураций указать невозможные и объяснить причину невозможности их реализации: а) 1р3; б) 3р6; в) 3s2; г) 2s2; д) 2d5; е) 5d2; ж) 3f12; з) 3p7.
28.Написать электронные формулы атомов элементов четвертого периода – калия, марганца, криптона. К какому семейству элементов они относятся?
29.Написать электронные формулы атомов элементов четвертого периода – скандия, цинка, мышьяка. К какому семейству элементов они относятся?
30.Назвать элементы 4, 5 и 6-го периодов, у которых заканчивается заполнение d-орбиталей (3d10, 4d10 и 5d10). Написать электронные формулы атомов этих элементов и указать, к какому периоду, группе и подгруппе периодической системы они относятся.
31.Запишите общую сокращенную электронную конфигурацию галогенов.
32.Сколько валентных электронов у атома фосфора?
33.Запишите полную электронную конфигурацию атома марганца. К семейству каких элементов он относится?
34.К какому семейству элементов относится группа элементов, имеющая общую сокращенную конфигурацию ns2np2?
35.Структура валентного электронного уровня атома элемента выражается формулой: a) 5s25p4;
36.б) 3d54s1. Определите порядковый номер и название элемента.
37.Какое максимальное число электронов может содержать атом на электронном уровне с главным квантовым числом n = 5 и n = 3?
38.Напишите электронные формулы атомов элементов с порядковыми номерами 24 и 33. Составьте их графические схемы. К какому электронному семейству относится каждый из них, почему?
39.Сколько неспаренных электронов содержат невозбужденные атомы В, S, Сr? Составьте их электронные и графические схемы.
40.Составьте электронные формулы атомов элементов с порядковым номером 32 и 42. У последнего один 5s-электрон проваливается на 4d-подуровень. К какому электронному семейству они относятся?
41.Какой подуровень заполняется в атомах после заполнения 5p-подуровня; после заполнения 5d-подуровня, почему?
42.Какие из электронных формул, отражающих строение невозбужденного атома некоторого элемента, неверны: а) 1s22s22p53s1; б) 1s22s22p6; в) 1s22s22p63s23p63d4;г) 1s22s22p63s23p64s2; д) 1s22s22p63s23d2? Почему?
43.Запишите электронные формулы атомов элементов с зарядом ядра 8; 13 и 18. Составьте графические схемы.
44.Какое максимальное количество электронов может располагаться в s-, p-, d- и f-подуровнях данного уровня? Почему? Напишите электронную структуру атома с порядковым номером 29.
45.Электронная структура атома описывается формулой 1s22s22p63s23p64s2. Какой это элемент? Составьте его графическую схему.Какое максимальное число электронов может содержать атом на электронном уровне с главным квантовым числом n = 5 и n = 3? Ответ мотивируйте.
46.Напишите электронные формулы атомов элементов с порядковыми номерами 24 и 33. Составьте их графические схемы. К какому электронному семейству относится каждый из них, почему?
Периодический закон и периодическая система элементов Д.И. Менделеева. Контрольные задании:
Периодический закон является главным инструментом систематизации и классификации химической информации, средствам направленного поиска соединений с ранее заданными свойствами.
Современная формулировка периодического закона: свойства химических элементов, а также формы и свойства их соединений находятся в периодической зависимости от величины заряда ядер их атомов.
Физический смысл периодического законы: при последовательном увеличении зарядов атомных ядер периодически повторяется конфигурация электронных оболочек, и как следствие, периодически повторяются химические свойства элементов.
Основные понятия и определения.
| Химический элемент | -вид атомов с одинаковым положительном зарядом ядра |
| Порядковый номер элемента | - номер в таблице Менделеева, соответствующий заряду атомного ядра |
| Период | - горизонтальный ряд элементов, расположенных в порядке возрастания зарядов ядер их атомов, электронная конфигурация их внешнего энергетического уровня которых изменяется от ns1 до ns2np 6 |
| Группа | - вертикальный ряд элементов, имеющих одинаковую электронную конфигурацию |
| Главная подгруппа | - последовательность элементов, у которых заполняется s- и p-подуровни внешних энергетических уровней, их начинают элементы 2 – 3 периодов |
| Побочная подгруппа | - последовательность элементов, у которых происходит заполнение внутренних (n-1)d- и (n-2)f- подуровней |
| Изоэлектронные атомы | - атомы, имеющие одинаковую электронную конфигурацию одноименных оболочек при разных значениях главного квантового числа n и проявляющие сходные химические свойства ( т.е расположенные в одной группе) |
Свойства атомов элементов и периодичность их изменения:
| Свойство | Определение (ед.изм.) | Изменение | |
| по периоду | по главной группе | ||
| Атомный радиус | Орбитальный – расстояние от ядра до более удаленного максимума электронной плотности (нм). Эффективный – половина расстояния между центрами двух смежных атомов в кристалле (нм). | уменьшается | увеличивается |
| Энергия ионизации | - минимальная энергия, необходимая для отрыва наиболее слабого связанного электрона от невозбужденного атома (I, кДж/моль, эВ) | увеличивается | уменьшается |
| Сродство к электрону | - энергетический эффект присоединения к атому одного электрона ( Е, кДж/моль, эВ) | увеличивается | уменьшается |
| Электроотрицательность | - способность атома в молекуле или кристалле притягивать к себе электроны, осуществляющие химическую связь
( ЭО=  ; отн.ед.)
Чем больше величина ЭО элемента, тем сильнее его неметаллические и химические свойства ; отн.ед.)
Чем больше величина ЭО элемента, тем сильнее его неметаллические и химические свойства
| увеличивается | уменьшается |
Последнее изменение этой страницы: 2016-07-23
lectmania.ru. Все права принадлежат авторам данных материалов. В случае нарушения авторского права напишите нам сюда...