
Категории:
ДомЗдоровьеЗоологияИнформатикаИскусствоИскусствоКомпьютерыКулинарияМаркетингМатематикаМедицинаМенеджментОбразованиеПедагогикаПитомцыПрограммированиеПроизводствоПромышленностьПсихологияРазноеРелигияСоциологияСпортСтатистикаТранспортФизикаФилософияФинансыХимияХоббиЭкологияЭкономикаЭлектроника
Типы химической связи. Строение молекул.
Виды гибридизации.
Свойства веществ, их реакционная способность зависит от состава, строения и типа химической связи между атомами. Все многочисленные химические процессы происходят в результате перегруппировок атомов, сопровождающихся разрывом старых связей между ними и образованием новых. Изучение химической связи, ее природы и свойств является фундаментальной задачей по химии.
Основные понятия и определения:
| Энергия связи | - энергия, затрачиваемая на разрыв химической связи ( кДж/моль) |
| Длина связи | - межъядерное расстояние между химически связанными атомами |
| Валентный угол | - угол между направлениями химической связи |
| Валентность | - число орбиталей атомов, принимающих участие в образовании химических связей |
| Кратность связи | - число электронных пар, связывающих два атома |
| Связывающая молекулярная орбиталь орбиталь (МО) | - область пространства между ядрами атомов, в которой вероятность нахождения электрона максимальна; энергия связывающей МО меньше энергии атомных орбиталей (АО) |
| Разрыхляющая МО | - область пространства между атомов с малой вероятностью нахождения электрона; энергия разрыхляющей МО больше энергии АО |
| Гибридизация | - геометрическое видоизменение АО, смешение и выравнивание их по форме и энергии |
| Геометрическая конфигурация молекулы | - взаимное пространственное расположение ее атомов, которое определяется длинами связи и валентными углами |
| Направленность ковалентной связи | - строго определенные значения валентных углов между связями в молекуле |
| Насыщенность ковалентной связи | - способность атомов к образованию строго определенного числа связей |
| Полярность ковалентной связи | - смещение электронной пары к более электроотрицательному атому |
| Диполь | - полярная молекула |
| Поляризуемость | - способность молекул ( и отдельных связей) поляризоваться под действием внешнего электрического поля |
Классификация типов химических связей:
| Характеристика | Пространственная направленность | Частицы, соединяемые данной связью |
| Ковалентная связь | ||
| Электронная пара является общей для двух атомов | Есть | Атомы неметаллов |
| Ионная связь | ||
| Между положительно и отрицательно заряженными ионами действуют электростатические силы | Нет | Катионы металлов и ионы неметаллов |
| Металлическая связь | ||
| Катионы металлов располагаются упорядоченно в поле внешних электронов, образующих «электронный газ» | Нет | Атомы металлов |
| Межмолекулярные силы | ||
| Возникают между молекулами и действуют на сравнительно малом расстоянии (ориентационные, индукционные, дисперсионные) | В некоторой степени | Полярные молекулы, полярные и неполярные молекулы, неполярные молекулы |
Основные положения метода ВС
1.В соответствии с принципом Паули химическая связь образуется за счет обобществления пар электронов с антипараллельними спинам;
2.Ковалентная связь является тем более прочной, чем более полно перекрываются АО;
3.Ковалентная связь направлена в сторону максимального перекрывания орбиталей, образующих молекулу.
Описание связей в гомоядерных двухатомных молекулах элементов второго периода по методу ВС
| Молекула | Электронная конфигурация атома | Схема связи | Кратность связи |
| Li2 | 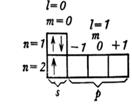
| Li :Li | |
| Be2 | 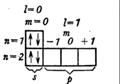
| :Be Be: | |
| B2 | 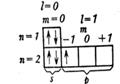
| :B: B: | |
| C2 | 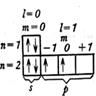
| :C::C: | |
| N2 | 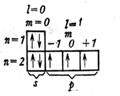
| :N 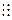 N: N:
| |
| O2 | 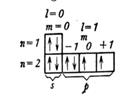
| .. .. :O::O: | |
| F2 | 
| .. .. :F :F: .. .. | |
| Ne2 | 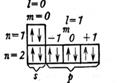
| .. .. :Ne ::Ne: .. .. |
| Тип гибридизации центрального атома | Пространственная конфигурация молекулы | Тип молекулы |
| sp | Линейная | АВ2 |
| sp2 dp2 | треугольная | АВ3 |
| sp3 | Тетраэдрическая Треугольно – пирамидальная угловая | АВ4 АВ3 АВ2 |
| dsp3 sp3d | Тригональная - бипирамидальная | АВ5 |
| d2sp3 sp3d2 | октаэдрическая | АВ6 |
Основные положения метода МО
1.При образовании молекулы происходит обобществление всех ядер и электронов.
2.Каждому электрону в молекуле соответствует молекулярная орбиталь подобно тому, как каждому электрону атоме соответствует атомная орбиталь.
3.Молекулярная орбиталь представляет собой линейную комбинацию (сложение и вычитание) атомных орбитателей.
Контрольные задания:
1.Дайте определения понятия ковалентная связь. Перечислите ее параметры и свойства.
2.С позиции метода валентных связей (ВС) объясните строение молекулы воды. Сколько градусов составляют валентные углы в этом соединении.
3.Дайте определения понятия насыщенности ковалентной связи. Подтвердите примерами.
4.Дайте определения понятия полярности связи. Определите тип химической связи в молекулах: N2, H2O, CCI4, SiH4, HF. Сколько градусов составляют валентные углы в этих соединениях.
5.Опишите обменный и донорно-акцепторный механизм образования ковалентной связи. Приведите примеры. Укажите донор и акцептор при образовании ионов: H3O+,NH4-, BF4-. Сколько градусов составляют валентные углы в этих соединениях.
6.Дайте определения понятия σ– B 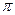 - связи. Объясните на примере молекулы азота понятия кратности связи.
- связи. Объясните на примере молекулы азота понятия кратности связи.
7.Напишите электронно-графические формулы атома хлора в нормальном и возбужденном состояниях. Укажите минимальную и максимальную валентность хлора, обусловленную неспаренными электронами, и приведите примеры соединений, в которых она реализуется.
8.Напишите электронно-графические формулы атома серы в нормальном и возбужденном состояниях. Чему равно валентность серы в H2SO4 и H2S?
9.Дайте понятие дипольного момента. Укажите, какая из молекул: HF, HCI, HBr, HI – характеризуется наименьшей величиной дипольного момента.
10.Дайте определения понятия гибридизации атомных орбиталей (АО). Объясните причину и механизм гибридизации, а также влияние типа гибридизации АО на пространственное строение молекулы. Приведите примеры.
11.Определите тип гибридизации АО бериллия, бора, углерода и кислорода в молекулах: BeCI2, BF3, CH4, H2O. Охарактеризуйте пространственное строение молекул.
12.Укажите тип кристаллической решетки и характер связи в кристаллах NaCI и Na. Чему равно координационное число натрия в этих решетках?
13.Дайте определение водородной связи, приведите примеры. Объясните причину того, что H2O и HF, имея меньшие молекулярные массы, чем H2Sи HCI, плавятся и кипят при более высоких температурах.
14.Дайте определения понятия ионной связи, опишите механизм ее образования и свойства. Приведите примеры ионных соединений. Напишите электронные формулы ионов Са2+, S2-, F-.
15.Дайте определения понятия степени окисления. Опрепеделите степень окисления углерода, его валентность в соединениях: CH4, CH3ОН, НСООН, СО, СО2, С2Н2.
16.Охарактеризуйте типы межмолекулярного взаимодействия (силы Ван – дер - Ваальса), природу и механизм его возникновения.
17.Спозиции метода ВС укажите, какие электроны атома брома участвуют в образовании ковалентной связи, определите тип гибридизации АО бора в молекуле BF3 и охарактеризуйте пространственное строение этой молекулы.
18.На основе метода валентных связей объясните механизм образования связи в молекуле СО.
19.Объясните, почему для элементов Р, S,CI максимальная валентность совпадает с номером групп , а для N,О,F она меньше, чем номер групп.
20.Напишите графические формулы оксидов углерода (II) и углерода (IV). Укажите валентность и степени окисления элементов в этих соединениях. Сколько градусов составляют валентные углы в этих соединениях.
Тема № 7.
Последнее изменение этой страницы: 2016-07-23
lectmania.ru. Все права принадлежат авторам данных материалов. В случае нарушения авторского права напишите нам сюда...